题目内容
7. 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.(1)Y原子核外共有7种不同运动状态的电子,基态T原子有7种不同能级的电子.
(2)X、Y、Z的第一电离能由小到大的顺序为C<O<N(用元素符号表示).
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为sp杂化.
(4)Z与R能形成化合物甲,1mol甲中含4 mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为SiF4的正四面体形、H2O为V形.
(5)G、Q、R氟化物的熔点如表,造成熔点差异的原因为NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低,Mg2+的半径比Na+的半径小,且Mg2+电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高.
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1 539 | 183 |
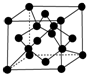
(7)X单质的晶胞如图所示,一个X晶胞中有8个X原子;若X晶体的密度为ρ g•cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个X原子之间的距离为$\frac{3}{4}$$\root{3}{\frac{12}{P{N}_{A}}}$ cm(用代数式表示).
分析 X的一种氢化物分子中既有σ键又有π键,说明分子里有双键或参键,X的一种氢化物为1:2型且所有原子共平面,所以X应为C元素,它的1:2型氢化物为乙烯;Z的L层上有2个未成对电子,即核外电子排布为1s22s22p2或1s22s22p4,X、Y、Z原子序数依次增大,所以Z为O元素,且Y为N元素;Q原子s能级与p能级电子数相等,则Q的核外电子排布为1s22s22p4或1s22s22p63s2,由于Q的原子序数比氧大,所以Q的电子排布为1s22s22p63s2,即Q为Mg;而G为金属元素,且原子序数介于氧和镁元素之间,所以G为Na;R单质是制造各种计算机、微电子产品的核心材料,则R为Si;T处于周期表的ds区,原子中只有一个未成对电子,价电子排布为3d104s1,故T为Cu.
解答 解:X的一种氢化物分子中既有σ键又有π键,说明分子里有双键或参键,X的一种氢化物为1:2型且所有原子共平面,所以X应为C元素,它的1:2型氢化物为乙烯;Z的L层上有2个未成对电子,即核外电子排布为1s22s22p2或1s22s22p4,X、Y、Z原子序数依次增大,所以Z为O元素,且Y为N元素;Q原子s能级与p能级电子数相等,则Q的核外电子排布为1s22s22p4或1s22s22p63s2,由于Q的原子序数比氧大,所以Q的电子排布为1s22s22p63s2,即Q为Mg;而G为金属元素,且原子序数介于氧和镁元素之间,所以G为Na;R单质是制造各种计算机、微电子产品的核心材料,则R为Si;T处于周期表的ds区,原子中只有一个未成对电子,价电子排布为3d104s1,故T为Cu.
(1)Y为N元素,核外电子排布式为1s22s22p3,所以7种不同运动状态的电子;T为Cu元素,它的核外电子排布式为:1s22s22p63s23p63d104s1,所以它有7个能级,
故答案为:7;7;
(2)C、N、O位于元素周期表同一周期,同周期随原子序数增大,第一电离能呈增大趋势,但N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:C<O<N,故答案为:C<O<N;
(3)OCN-与CO2互为等电子体,所以它们结构相似,OCN-中C原子与O、N原子之比分别形成2对共用电子对,没有孤电子对,所以碳的杂化方式为sp杂化,
故答案为:sp杂化;
(4)Z与R能形成化合物甲为二氧化硅,在二氧化硅晶体中,每个硅原子周围有四个Si-O键,所以1mol二氧化硅中含有4molSi-O键;
SiO2与HF反应的方程式为:SiO2+4HF=SiF4+2H2O,其中SiF4中硅原子的价层电子对数为:4+$\frac{4-1×4}{2}$=4,没有孤对电子,所以SiF4的空间构型为正四面体、H2O为V形故答案为:4;SiF4的正四面体形、H2O为V形;
(5)在NaF、MgF2、SiF4中,NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点最低,Mg2+的半径比Na+的半径小,且Mg2+电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高,
故答案为:NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低,Mg2+的半径比Na+的半径小,且Mg2+电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高;
(6)向硫酸铜溶液中逐滴加入氨水溶液至过量,反应生成四氨合铜络离子,反应的离子方程式为:Cu2++4NH3.H2O=[Cu(NH3)4]2++4H2O,
故答案为:Cu2++4NH3.H2O=[Cu(NH3)4]2++4H2O;
(7)碳单质的晶胞为 ,晶胞中含有C原子数目为4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,C原子与周围4个原子形成正四面体,正四面体中心C原子与顶点碳原子相邻,距离最近,晶胞质量为8×$\frac{12}{{N}_{A}}$g,晶体的密度为p g/cm3,则晶胞棱长为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm,则正四面体的棱长为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$,则正四面体的斜高为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$×$\frac{\sqrt{3}}{2}$,令斜高为为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$×$\frac{\sqrt{3}}{2}$=bcm,底面中心到边的距离为$\frac{1}{3}$b,设正四面体的高为a cm,则a2+($\frac{1}{3}$b)2=b2,解得a=$\frac{\sqrt{6}}{3}b$,故正四面体中心原子到顶点距离为$\frac{3}{4}$a=$\frac{3}{4}$×$\frac{\sqrt{6}}{3}b$=$\frac{3}{4}$×$\frac{\sqrt{6}}{3}$×$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$×$\frac{\sqrt{3}}{2}$=$\frac{3}{4}$$\root{3}{\frac{12}{P{N}_{A}}}$cm,故答案为:8;$\frac{3}{4}$$\root{3}{\frac{12}{P{N}_{A}}}$cm.
,晶胞中含有C原子数目为4+8×$\frac{1}{8}$+6×$\frac{1}{2}$=8,C原子与周围4个原子形成正四面体,正四面体中心C原子与顶点碳原子相邻,距离最近,晶胞质量为8×$\frac{12}{{N}_{A}}$g,晶体的密度为p g/cm3,则晶胞棱长为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm,则正四面体的棱长为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$,则正四面体的斜高为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$×$\frac{\sqrt{3}}{2}$,令斜高为为$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$×$\frac{\sqrt{3}}{2}$=bcm,底面中心到边的距离为$\frac{1}{3}$b,设正四面体的高为a cm,则a2+($\frac{1}{3}$b)2=b2,解得a=$\frac{\sqrt{6}}{3}b$,故正四面体中心原子到顶点距离为$\frac{3}{4}$a=$\frac{3}{4}$×$\frac{\sqrt{6}}{3}b$=$\frac{3}{4}$×$\frac{\sqrt{6}}{3}$×$\root{3}{\frac{\frac{8×12}{{N}_{A}}}{P}}$cm×$\frac{\sqrt{2}}{2}$×$\frac{\sqrt{3}}{2}$=$\frac{3}{4}$$\root{3}{\frac{12}{P{N}_{A}}}$cm,故答案为:8;$\frac{3}{4}$$\root{3}{\frac{12}{P{N}_{A}}}$cm.
点评 本题是对物质结构的考查,涉及电离能、杂化轨道、分子结构、晶体类型与性质、配合物、晶胞计算等,(7)中晶胞计算为易错点、难点,需要学生具备一定的空间想象与数学计算能力,关键理解距离最近碳原子位置.

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案| A. | 所得溶液中水电离出c(OH-)=1.0×10-10mol•L-1 | |
| B. | 所得溶液中的c(Cu2+)=1.0×10-5mol•L-1 | |
| C. | 向所得溶液中滴加Na2S溶液会有黑色沉淀出现 | |
| D. | 除去工业废水中的Cu2+,可以用FeS作沉淀剂 |
 已知某密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g),的平衡物质的量浓度c(CO2)与温度t的关系如图所示.下列说法错误的是( )
已知某密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g),的平衡物质的量浓度c(CO2)与温度t的关系如图所示.下列说法错误的是( )| A. | 平衡状态A与C相比,平衡状态A的c(CO)较小 | |
| B. | 在t2时,D点的反应速率:ν(逆)>ν(正) | |
| C. | 反应CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 | |
| D. | 若t1、t2时的平衡常数分别为K1、K2,则K1<K2 |
| A. | 1 molNa2O2和水完全反应,转移电子数为2NA | |
| B. | 0.5 L 0.2 mol•L-1FeCl3溶液中,含Fe3+离子数为0.1 NA | |
| C. | 理论上氢氧燃料电池负极消耗11.2 L标准状况下气体,外线路通过电子数为NA | |
| D. | 常温常压下,28 g乙烯和丙烯混合气体含有的碳原子总数为2.5NA |
| A. | 医用酒精的浓度通常为95% | |
| B. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| C. | 将水坝的钢铁闸门与直流电的正极相连可以防闸门腐蚀 | |
| D. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 |
探究一:称取粗铁粒10 g放入某浓度硝酸中,充分反应后得到溶液X并收集到气体Y.为了探究溶液X中铁的价态,同学甲设计如下实验:
现有药品和仪器:药品有:0.1 mol/L KSCN溶液,0.1 mol/L KI溶液,0.2 mol/L酸性高锰酸钾溶液,氯水等;器材有:试管和滴管.
(1)请你设计简单实验,探究上述猜想是否正确,填写下列实验报告.
| 实验步骤 | 操作 | 现象与结论 | 离子方程式 |
| 第一步 | 取少量溶液装于试管,向试管中加入几滴KSCN溶液 | ||
| 第二步 | 若溶液紫色褪去,则溶液含有Fe2+;若无明显变化,则不含Fe2+ |
(3)装置丙收集满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定气体Y中含NO?说明理由不能确定,由于NO2与水反应也能生成NO,故不能确定气体Y中含NO.
(4)同学丙对同学乙的实验设计提出了质疑,他认为丙中的现象不足以证明NO存在,稍作改进即可.试回答改进措施:
(5)同学丁为了探究气体Y的组成,将224mL气体Y通入足量的NaOH溶液中,气体被完全吸收,所得溶液再用0.15mol/L 酸性KMnO4溶液滴定,消耗20mL KMnO4溶液.则气体Y中NO、NO2的体积比为:1:3.
(已知2NO2+2NaOH═NaNO3+NaNO2+H2O和NO2+NO+2NaOH═2NaNO2+H2O)
| A. | 常温下,1L0.1mol•L-1NaClO溶液中阴离子总数大于0.1NA | |
| B. | 7.8gNa2O2中含有的阴、阳离子总数是0.3NA | |
| C. | N2H2分子中各原子的最外层(除H外)均为8电子结构,1molN2H2中有共用电子对数目为3NA | |
| D. | 50mL18mol•L-1浓硫酸与足量铜反应,转移电子数小于0.9NA |
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.(1)如图是1mol NO2气体和1mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1;
已知:N2 (g)+2NO2 (g)?4NO(g)△H=+292.3kJ•mol-1,
则反应:2NO(g)+2CO(g)?N2(g)+2CO2(g) 的△H=-760.3KJ/mol;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20mol NO2和5mol O2发生反应:4NO2(g)+O2(g)?2N2O5(g);已知体系中n(NO2)随时间变化如下表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
②反应达到平衡后,NO2的转化率为49.6%,若要增大NO2的转化率,可采取的措施有AD
A.降低温度 B.充入氦气,使体系压强增大
C.再充入NO2 D.再充入4mol NO2和1mol O2.
| A. | 用小刀切割钠块 | B. | 钠沉于水中 | ||
| C. | 钠熔化成小球 | D. | 发出“嘶嘶”的响声 |