题目内容
12. 如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )| A. | Y元素的两种同素异形体在常温下都是气体 | |
| B. | 原子半径由大到小排列顺序Z>Y>X | |
| C. | 最高价氧化物对应水化物的酸性W>Z | |
| D. | 阴离子半径由大到小排列顺序X>Y>Z>W |
分析 X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的$\frac{7}{10}$,则W原子其内层电子总数为10,最外层电子数为7,故W是Cl元素,结合X、Y、Z、W在周期表中的位置关系可知,Z为S元素,Y为O元素,X为N元素,然后结合元素周期律的递变规律来解答.
解答 解:X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的$\frac{7}{10}$,则W原子其内层电子总数为10,最外层电子数为7,故W是Cl元素,结合X、Y、Z、W在周期表中的位置关系可知,Z为S元素,Y为O元素,X为N元素,
A.Y元素的两种同素异形体为氧气、臭氧,在常温下都是气体,故A正确;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径由大到小排列顺序Z>X>Y,故B错误;
C.非金属性Cl>S,则最高价氧化物对应水化物的酸性W>Z,故C正确;
D.电子层越多,离子半径越大,具有相同电子排布的离子中原子序数大的离子半径小,则阴离子半径由大到小排列顺序Z>W>X>Y,故D错误;
故选BD.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
2.下列有关物质用途的说法中,正确的是( )
| A. | 工业上利用氨气制硝酸属于人工固氮 | |
| B. | 明矾能够消毒杀菌是利用了胶体的吸附性 | |
| C. | 常温下,运输浓H2SO4、浓HNO3时可用铝制或铁制槽车 | |
| D. | 硅可用于制造光导纤维 |
3.化学与材料、生活和环境密切相关.下列有关说法中正确的是( )
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 酸性高锰酸钾溶液应装在酸式滴定管中,原因是酸性高锰酸钾能氧化橡胶 | |
| C. | 植物油和裂化汽油都能使溴水褪色,原理是不同的 | |
| D. | 明矾能够用于净水,是因为明矾的溶液是酸性的 |
20.高纯度晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”.它可以按下列方法制备: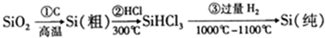 ,下列说法正确的是( )
,下列说法正确的是( )
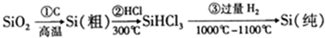 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 步骤①的化学方程式为:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| B. | 步骤①②③中每生成或反应1mol Si,转移2mol电子 | |
| C. | 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应 | |
| D. | SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3 |
7.铜锌原电池工作时,下列叙述正确的是( )
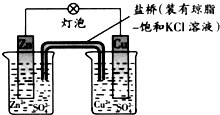

| A. | 正极反应为:Zn-2e-═Zn2+ | B. | 在外电路中,电子从铜片流向锌片 | ||
| C. | 负极发生还原反应 | D. | 盐桥中的K+移向CuSO4溶液 |

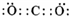 .
.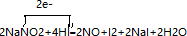 .
.