题目内容
15.下列每组物质中含有的化学键类型相同的是( )| A. | NaCl、HCl、H2O、NaOH | B. | Cl2、Na2S、HCl、CO2 | ||
| C. | HBr、CCl4、H2O、CO2 | D. | Na2O2、H2O2、H2O、O2 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA、第IIA族和第VIA、第VIIA族元素之间易形成离子键.
解答 解:A.NaCl中只含离子键、NaOH中既含共价键又含离子键,HCl和H2O只含共价键、故A错误;
B.Na2S只存在离子键,Cl2、HCl、CO2只存在共价键,故B错误;
C.HBr、CCl4、H2O、CO2分子中只存在共价键,故C正确;
D.Na2O2中既有离子键又有共价键,而H2O2、H2O、O2分子中只存在共价键,故D错误;
故选C.
点评 本题考查了化学键的判断,根据物质的构成微粒及微粒间的作用力来分析解答,明确离子键和共价键概念的内涵及区别,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列叙述不正确的是( )
| A. | c(NH4+)相等的NH4HCO3溶液、(NH4)2Fe(SO4)2溶液和(NH4)2SO4溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4HCO3) | |
| B. | 常温下,0.1 mol•L-1HCl溶液与等体积0.1 mol•L-1Ba(OH)2溶液混合后,溶液的pH=13 | |
| C. | 常温下,由水电离产生的c(H+)=10-13 mol•L-1的溶液,Fe2+、NO3-、Cl-、SO42-一定不能大量共存 | |
| D. | 0.1 mol•L-1的NaHCO3溶液中,c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
13.某无色透明溶液,能与铝作用放氢气,则此溶液中一定可以大量共存的离子组是( )
| A. | K+、Na+、Cl- | B. | K+、Cu2+、SO42- | C. | Cl-、NO3-、Mg2+ | D. | Ba2+、SO42-、Na+ |
3.在20℃时某化学反应的速率为0.15mol•L-1•s-1,若温度每升高5℃,反应速率提高到原来的2倍,则为使反应速率达到1.2mol•L-1•s-1,应使反应在什么温度下进行( )
| A. | 30℃ | B. | 35℃ | C. | 40℃ | D. | 45℃ |
7.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 一定条件下,1 mol N2和3 mol H2充分反应,生成物中的N-H键数目为6NA | |
| B. | 9.2g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2NA | |
| C. | 完全燃烧1.5 molCH3CH2OH和C2H4的混合物,转移电子数为18NA | |
| D. | 1 L 0.1mol L-1的Na2S溶液中S2-和HS-的总数为0.1NA |
4.下列说法正确的是( )
| A. | CO是酸性氧化物 | B. | BaSO4 是强电解质 | ||
| C. | 氢氧化铁胶体属于纯净物 | D. | 纯碱属于碱类物质 |
5.一定能使化学反应速率加快的因素是( )
①扩大容器容积
②使用正催化剂
③增大反应物的物质的量
④升高温度
⑤缩小容积
⑥增大压强.
①扩大容器容积
②使用正催化剂
③增大反应物的物质的量
④升高温度
⑤缩小容积
⑥增大压强.
| A. | ②③ | B. | ②③④⑥ | C. | ②③③⑤ | D. | ②④ |
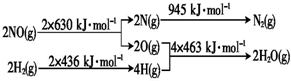
 .C2A4的水溶液呈碱(填“酸”“碱”或“中”)性,1mol C2A4最多可以与2mol HCl或NaOH发生中和反应生成正盐.C2A4 和A2D2 既具有氧化性,又具有还原性,从化合价的角度解释C2A4 和A2D2 既具有氧化性又具有还原性的原因N2H4中N显-2,H2O2中O显-1,均为相应元素的中间价态,所以既有氧化性,又有还原性
.C2A4的水溶液呈碱(填“酸”“碱”或“中”)性,1mol C2A4最多可以与2mol HCl或NaOH发生中和反应生成正盐.C2A4 和A2D2 既具有氧化性,又具有还原性,从化合价的角度解释C2A4 和A2D2 既具有氧化性又具有还原性的原因N2H4中N显-2,H2O2中O显-1,均为相应元素的中间价态,所以既有氧化性,又有还原性 ,该化合物与CA3和A2D的熔点由高到低的顺序为H2O>NH3>CH4(用化学式表示).
,该化合物与CA3和A2D的熔点由高到低的顺序为H2O>NH3>CH4(用化学式表示).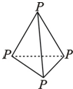 .CA3、A2D、EA3的热稳定性由强到弱的顺序为H2O>NH3>PH3(用化学式表示).
.CA3、A2D、EA3的热稳定性由强到弱的顺序为H2O>NH3>PH3(用化学式表示).