题目内容
5.一定能使化学反应速率加快的因素是( )①扩大容器容积
②使用正催化剂
③增大反应物的物质的量
④升高温度
⑤缩小容积
⑥增大压强.
| A. | ②③ | B. | ②③④⑥ | C. | ②③③⑤ | D. | ②④ |
分析 增大反应物浓度、升高温度、使用催化剂等均可加快反应速率,以此来解答.
解答 解:①反应有气体参加,则扩大容器的容积,速率减小,而固体和液体基无影响,故不选;
②使用催化剂,降低反应需要的活化能,反应速率加快,故选;
③增加反应物的物质的量,浓度增大,反应速率加快,如果反应物中有固体物质,增加固体的量无影响,故不选;
④升高温度,反应速率加快,故选;
⑤缩小容积,则浓度增大,反应速率加快,但对于无气体参加的反应无影响,故不选;
⑥增大容器内的压强,若恒容充入稀有气体,反应速率不变,故不选;
故选D.
点评 本题考查影响化学反应速率的因素,为高频考点,把握影响反应速率的因素为解答的关键,侧重常见外因对反应速率影响的考查,注意反应为有气体参加的反应,题目难度不大.

练习册系列答案
相关题目
15.下列每组物质中含有的化学键类型相同的是( )
| A. | NaCl、HCl、H2O、NaOH | B. | Cl2、Na2S、HCl、CO2 | ||
| C. | HBr、CCl4、H2O、CO2 | D. | Na2O2、H2O2、H2O、O2 |
16.下列有关叙述正确的是( )
| A. | 在反应BrCl+H2O═HCl+HBrO中,BrCl既是氧化剂又是还原剂 | |
| B. | 双氧水与高锰酸钾酸性溶液反应:2KMnO4+3H2O2+3H2SO4═K2SO4+2MnSO4+4O2↑+6H2O | |
| C. | K37ClO3与H35Cl反应的化学方程式为K37ClO3+6H35Cl═K37Cl+335Cl2↑+3H2O | |
| D. | 在反应CH3CH2OH+K2Cr2O7(H+)→CH3COOH中,每消耗1mol乙醇转移4NA个电子(NA为阿伏伽德罗常数的值) |
20.N、P等同主族元素形成的同一类型化合物,往往其结构和性质相似.下列对PH4Cl的叙述中,正确的是( )
| A. | 它是一种共价化合物 | B. | 它既含离子键又含共价键 | ||
| C. | 它可能能与NaOH溶液反应 | D. | 它与H2O2所含化学键完全相同 |
10.由A、B、C、D四种金属按表中装置进行实验.
根据实验现象回答下列问题:
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
| 装置 | 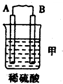 | 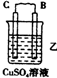 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
17.将1mol乙醇(其中的氧用18O标记)在浓硫酸存在条件下与足量乙酸充分反应.下列叙述不正确的是( )
| A. | 生成的乙酸乙酯中含有18O | |
| B. | 能生成乙酸乙酯的质量为88g | |
| C. | 生成乙酸乙酯的质量为90g | |
| D. | 反应后的混合物中有两种物质含18O |
14.已知:H2(g)+F2(g)═2HF(g)△H=-270kJ•mol-1,下列说法正确的是( )
| A. | 2 L氟化氢气体分解成1L氢气与1L氟气吸收270kJ热量 | |
| B. | 1mol氢气与1mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| C. | 在相同条件下,1mol氢气与1 mol氟气的总能量大于2mol氟化氢气体的能量 | |
| D. | 1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270kJ热量 |
6.下列各组中两种微粒所含电子数不相等的是( )
| A. | H3O+和OH- | B. | CO和N2 | C. | HNO3和NO3- | D. | CH3+和NH4+ |
