题目内容
下列离子方程式正确的是( )
| A、Fe和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | ||||
| B、Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | ||||
C、用石墨做电极电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
| D、强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:4OH-+3ClO-+2Fe(OH)3═2FeO42-+3Cl-+5H2O |
考点:离子方程式的书写
专题:
分析:A.反应生成硫酸亚铁和氢气;
B.电子、原子不守恒;
C.反应生成氢氧化镁沉淀和氢气、氯气;
D.发生氧化还原反应,遵循电子、电荷守恒.
B.电子、原子不守恒;
C.反应生成氢氧化镁沉淀和氢气、氯气;
D.发生氧化还原反应,遵循电子、电荷守恒.
解答:
解:A.Fe和稀硫酸反应的离子反应为Fe+2H+═Fe2++H2↑,故A错误;
B.Na2O2溶于水产生O2的离子反应为2Na2O2+2H2O═4Na++4OH-+O2↑,故B错误;
C.用石墨做电极电解饱和MgCl2溶液的离子反应为Mg2++2Cl-+2H2O
Cl2↑+H2↑+Mg(OH)2↓,故C错误;
D.强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4的离子反应为4OH-+3ClO-+2Fe(OH)3═2FeO42-+3Cl-+5H2O,故D正确;
故选D.
B.Na2O2溶于水产生O2的离子反应为2Na2O2+2H2O═4Na++4OH-+O2↑,故B错误;
C.用石墨做电极电解饱和MgCl2溶液的离子反应为Mg2++2Cl-+2H2O
| ||
D.强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4的离子反应为4OH-+3ClO-+2Fe(OH)3═2FeO42-+3Cl-+5H2O,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、电解的离子反应考查,题目难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列有关氧化还原反应说法正确的是( )
| A、工业制硫酸、工业制硝酸、由石英获取单晶硅变化均为氧化还原反应 |
| B、氧化反应与还原反应一定同时发生,但氧化剂、还原剂可不直接接触 |
| C、置换反应肯定都是氧化还原反应,但复分解反应可能是氧化还原反应 |
| D、氧化还原反应中氧化产物与还原产物不会再发生氧化还原反应 |
下列各组括号内的试剂,能用于除掉物质中杂质的是( )
| A、Fe粉中混有Zn粉杂质(稀H2SO4) |
| B、FeCl2中混有FeCl3杂质(Cl2) |
| C、CO气体中混有CO2杂质(NaOH溶液) |
| D、FeCl3中混有FeCl2杂质(铁屑) |
能证明淀粉已经完全水解的试剂是( )
| A、碘化钾溶液 | B、银氨溶液 |
| C、碘水 | D、酚酞试剂 |
下列说法不正确的是( )
| A、BaSO4、NaCl、NaHCO3均属于强电解质 |
| B、SO2、NO2、NO均属于二次污染物 |
| C、NaHCO3、NH4Cl、(NH4)2CO3三种固体受热后均无固体剩余 |
| D、FeCl2、NaHSO3、Fe(OH)3都可以通过化合反应直接制得 |
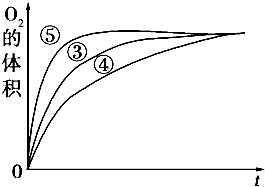 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.