题目内容
下列说法不正确的是( )
| A、BaSO4、NaCl、NaHCO3均属于强电解质 |
| B、SO2、NO2、NO均属于二次污染物 |
| C、NaHCO3、NH4Cl、(NH4)2CO3三种固体受热后均无固体剩余 |
| D、FeCl2、NaHSO3、Fe(OH)3都可以通过化合反应直接制得 |
考点:强电解质和弱电解质的概念,常见的生活环境的污染及治理,钠的重要化合物,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:A.酸碱盐都是电解质;
B.二次污染物是排入环境中的一次污染物在物理化学因素或微生物作用下发生变化所生成的新污染物;
C.根据受热分解的产物的熔点考虑;
D.Fe和FeCl3反应生成FeCl2;SO2和H2O、氢氧化钠反应生成NaHSO3;Fe(OH)2被氧化生成Fe(OH)3.
B.二次污染物是排入环境中的一次污染物在物理化学因素或微生物作用下发生变化所生成的新污染物;
C.根据受热分解的产物的熔点考虑;
D.Fe和FeCl3反应生成FeCl2;SO2和H2O、氢氧化钠反应生成NaHSO3;Fe(OH)2被氧化生成Fe(OH)3.
解答:
解:A.酸碱盐都是电解质,故A正确;
B.二次污染物是排入环境中的一次污染物在物理化学因素或微生物作用下发生变化所生成的新污染物,二氧化硫可由硫化氢燃烧得到,二氧化氮可由一氧化氮和氧气反应得到,一氧化氮可由氨气和氧反应得到,故都属于二次污染物,故B正确;
C.NaHCO3受热分解得到的碳酸钠熔点高,故有固体碳酸钠剩余,故C错误;
D.Fe和FeCl3反应生成FeCl2,方程式为Fe+2FeCl3=3FeCl2,所以能通过化合反应直接制得;SO2和氢氧化钠反应生成NaHSO3,方程式为SO2+NaOH=NaHSO3,所以能通过化合反应直接制得;Fe(OH)2被氧化生成Fe(OH)3,方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以能通过化合反应直接制得3,故D正确;
故选C.
B.二次污染物是排入环境中的一次污染物在物理化学因素或微生物作用下发生变化所生成的新污染物,二氧化硫可由硫化氢燃烧得到,二氧化氮可由一氧化氮和氧气反应得到,一氧化氮可由氨气和氧反应得到,故都属于二次污染物,故B正确;
C.NaHCO3受热分解得到的碳酸钠熔点高,故有固体碳酸钠剩余,故C错误;
D.Fe和FeCl3反应生成FeCl2,方程式为Fe+2FeCl3=3FeCl2,所以能通过化合反应直接制得;SO2和氢氧化钠反应生成NaHSO3,方程式为SO2+NaOH=NaHSO3,所以能通过化合反应直接制得;Fe(OH)2被氧化生成Fe(OH)3,方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以能通过化合反应直接制得3,故D正确;
故选C.
点评:本题考查了电解质的判断、常见污染物、元素化合物知识,较简单,注意知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式正确的是( )
| A、Fe和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | ||||
| B、Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | ||||
C、用石墨做电极电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
| D、强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:4OH-+3ClO-+2Fe(OH)3═2FeO42-+3Cl-+5H2O |
需要加入适当的氧化剂才能实现的反应( )
| A、SO3→HSO4- |
| B、MnO4-→Mn2+ |
| C、PCl3→PCl5 |
| D、CO2→H2CO3 |
下列说法正确的是( )
①NO2气体通入FeSO4溶液中无现象;
②SiC俗称金刚砂,可用作砂纸、砂轮的磨料;
③将过量CO2气体通入水玻璃溶液中可以看到有白色胶状沉淀生成;
④用铜片在加热的条件下就可鉴别浓硫酸和稀硫酸;
⑤将盛有10mlNO2和O2的混和气体的试管倒扣于水槽中一段时间后水面可能充满整个试管;
⑥70mL的H2S和90mL的O2混合点燃后恢复到原状况可产生70mL的SO2.
①NO2气体通入FeSO4溶液中无现象;
②SiC俗称金刚砂,可用作砂纸、砂轮的磨料;
③将过量CO2气体通入水玻璃溶液中可以看到有白色胶状沉淀生成;
④用铜片在加热的条件下就可鉴别浓硫酸和稀硫酸;
⑤将盛有10mlNO2和O2的混和气体的试管倒扣于水槽中一段时间后水面可能充满整个试管;
⑥70mL的H2S和90mL的O2混合点燃后恢复到原状况可产生70mL的SO2.
| A、①③④⑤ | B、②③④⑥ |
| C、①②⑥ | D、②③④⑤ |
居室空气污染物达300多种,其中有一种来自人造地板、家具以及装修粘合剂,长期接触可引起过敏性皮炎、免疫功能异常.该污染物是( )
| A、甲醛(HCHO) |
| B、CO |
| C、氡(Rn) |
| D、NO2 |
下列说法中不正确的是( )
| A、在非标准状况下,1 mol O2的体积也有可能是22.4 L |
| B、在温度和压强一定时,气态物质的体积主要由气体分子数目和分子的大小决定 |
| C、同温同压下,0.3 mol N2和0.7 mol O2的体积比为3:7 |
| D、同温同压下,相同体积的任何气体所含有的分子数目一定相同 |
反应A(g)+3B(g)?2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是( )
| A、v(A)=0.15 mol?L-1?min-1 |
| B、v(B)=0.015 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(D)=0.45 mol?L-1?min-1 |
下列离子反应方程式,书写正确的是( )
| A、碳酸氢钠溶液中加入醋酸:CO32-+2H+=H2O+CO2↑ |
| B、稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ |
| C、碳酸钙中加入盐酸:CO32-+2H+=H2O+CO2↑ |
| D、氢氧化钠溶液中加入硫酸:H++OH-=H2O |
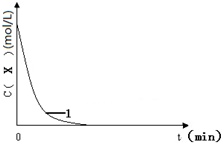 已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生.若再加入双氧水,将发生反应:H2O2+2H++2I-═2H2O+I2,且生成的I2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成的I2完全消耗.由于溶液中的I-继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝.因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I-═2H2O+I2的反应速率.
已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生.若再加入双氧水,将发生反应:H2O2+2H++2I-═2H2O+I2,且生成的I2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成的I2完全消耗.由于溶液中的I-继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝.因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I-═2H2O+I2的反应速率.