题目内容
下列离子方程式正确的是( )
| A、NaHCO3水解时的离子方程式:HCO3-+H2O?H3O++CO32- |
| B、AgCl溶于水时形成的溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq) |
| C、少量的CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O=2C6H5OH+CO32- |
| D、向NaHSO4溶液中滴加过量的Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、选项中是碳酸氢根离子的电离方程式;
B、依据沉淀溶解平衡分析判断;
C、苯酚显弱酸性和碳酸钠反应生成碳酸氢钠;
D、向NaHSO4溶液中滴加过量的Ba(OH)2溶液,硫酸氢钠全部反应,离子方程式中符合硫酸氢钠的组成比.
B、依据沉淀溶解平衡分析判断;
C、苯酚显弱酸性和碳酸钠反应生成碳酸氢钠;
D、向NaHSO4溶液中滴加过量的Ba(OH)2溶液,硫酸氢钠全部反应,离子方程式中符合硫酸氢钠的组成比.
解答:
解:A、选项中是碳酸氢根离子的电离方程式,水解离子方程式为:HCO3-+H2O?H2CO3+OH-,故A错误;
B、依据沉淀溶解平衡分析判断,AgCl溶于水时形成的溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq),故B正确;
C、苯酚显弱酸性和碳酸钠反应生成碳酸氢钠,反应的离子方程式:C6H5O-+CO2+H2O=C6H5OH+HCO3-,故C错误;
D、向NaHSO4溶液中滴加过量的Ba(OH)2溶液,硫酸氢钠全部反应,离子方程式中符合硫酸氢钠的组成比,反应的离子方程式H++SO42-+Ba2++OH-=BaSO4↓+H2O,故D错误;
故选B.
B、依据沉淀溶解平衡分析判断,AgCl溶于水时形成的溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq),故B正确;
C、苯酚显弱酸性和碳酸钠反应生成碳酸氢钠,反应的离子方程式:C6H5O-+CO2+H2O=C6H5OH+HCO3-,故C错误;
D、向NaHSO4溶液中滴加过量的Ba(OH)2溶液,硫酸氢钠全部反应,离子方程式中符合硫酸氢钠的组成比,反应的离子方程式H++SO42-+Ba2++OH-=BaSO4↓+H2O,故D错误;
故选B.
点评:本题考查了离子方程式书写方法和正误判断,主要是物质性质分析,量不同产物不同,题目难度中等.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
下列操作中,不正确的是( )
| A、苯酚沾在手上应立即用酒精洗涤 |
| B、燃着的酒精灯打翻起火,应用水扑灭 |
| C、实验收室进行石油分馏、制乙烯实验时,均需在反应器中加入少量碎瓷片 |
| D、点燃甲烷、乙烯等可燃性气体前必须先检验其纯度 |
下列各组离子,在强碱性溶液中可以大量共存的是( )
| A、K+、Ca2+、HCO3-、Cl- |
| B、Ba2+、Na+、AlO2-、NO3- |
| C、NH4+、Na+、NO3-、CO32- |
| D、Mg2+、Na+、Cl-、SO42- |
下列有关实验现象的描述中,正确的是( )


| A、如图所示装置中,锌电极上一定没有气泡生成 |
| B、向CaCl2饱和溶液中通入少量CO2,溶液中会出现白色沉淀 |
| C、做氯化铵分解实验时,加热试管底部,试管口处有晶体出现 |
| D、向蛋白质溶液中滴加足量饱和NaCl溶液的过程中无固体析出 |
 [化学--选修物质结构与性质]
[化学--选修物质结构与性质] ,由短周期元素构成的与SO
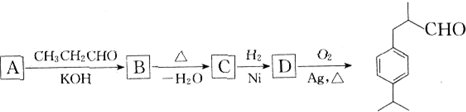
,由短周期元素构成的与SO )在食品、化妆品等工业中用作香料添加剂.其合成流程为(部分产物及反应条件已略去,键线式参见本试卷第12题):
)在食品、化妆品等工业中用作香料添加剂.其合成流程为(部分产物及反应条件已略去,键线式参见本试卷第12题):