题目内容
某些非金属单质可与水发生置换反应,如2F2+2H2O→4HF+O2.非金属单质与水发生置换反应的另一个熟知实例是(用热化学方程式表示,热值用Q表示,Q>0): .
考点:吸热反应和放热反应
专题:化学反应中的能量变化
分析:碳能与水反应生成一氧化碳和氢气,据此解题.
解答:
解:碳能与水反应生成一氧化碳和氢气:C(s)+H2O(g)
CO(g)+H2(g)-Q,故答案为:C(s)+H2O(g)
CO(g)+H2(g)-Q.
| 高温 |
| 高温 |
点评:本题考查常见的化学反应,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
在下列物质中,既具有氧化性又具有还原性的是( )
| A、铁 | B、硫 | C、铁和硫 | D、氢气 |
如图是印在食品包装内常见小袋子上的部分图案,该小袋子内的物质最有可能是( )


| A、铁粉 | B、氧化钠 |
| C、亚硫酸钠 | D、生石灰 |
下列叙述错误的是( )
| A、0.012kg12C中含有约6.02×1023个碳原子 |
| B、在同温同压下,1摩尔固体或液体的体积各不相同,1摩尔气体体积大约相等 |
| C、在使用摩尔表示物质的量的单位时,应指明粒子的种类 |
| D、只有在标准状况下,1摩尔气体积才约为22.4 L |

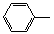 -CH=CH2)和D(HO-
-CH=CH2)和D(HO-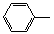 -CHO)按如下方法合成:
-CHO)按如下方法合成: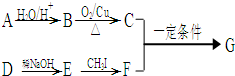
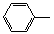 -ONa+RCH2I→
-ONa+RCH2I→ -OCH2R
-OCH2R