题目内容
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4 L 苯中含有NA个苯分子 |
| B、1 mol/L NaCl溶液含有NA个Na+ |
| C、1 mol Fe和足量稀硝酸反应产生22.4LNO |
| D、16 g CH4中含有4 NA个C-H键 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下,苯的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
B.缺少氯化钠溶液的体积,无法计算溶液中钠离子数目;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算一氧化氮的体积;
D.甲烷分子中含有4个碳氢键,16g甲烷的物质的量为1mol,含有4mol碳氢键.
B.缺少氯化钠溶液的体积,无法计算溶液中钠离子数目;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算一氧化氮的体积;
D.甲烷分子中含有4个碳氢键,16g甲烷的物质的量为1mol,含有4mol碳氢键.
解答:
解:A.标况下,苯不是气体,不能使用标况下的气体摩尔体积计算22.4L苯的物质的量,故A错误;
B.没有告诉1mol/L氯化钠溶液的体积,无法计算溶液中钠离子的物质的量及数目,故B错误;
C.1mol铁与足量稀硝酸完全反应失去3mol电子,生成1mol一氧化氮,由于没有告诉在标况下,无法计算1molNO的体积,故C错误;
D.16g甲烷的物质的量为1mol,1mol甲烷中含有4mol碳氢键,含有4 NA个C-H键,故D正确;
故选D.
B.没有告诉1mol/L氯化钠溶液的体积,无法计算溶液中钠离子的物质的量及数目,故B错误;
C.1mol铁与足量稀硝酸完全反应失去3mol电子,生成1mol一氧化氮,由于没有告诉在标况下,无法计算1molNO的体积,故C错误;
D.16g甲烷的物质的量为1mol,1mol甲烷中含有4mol碳氢键,含有4 NA个C-H键,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的综合应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,题中缺少氯化钠溶液的体积.

练习册系列答案
相关题目
下列物质不能发生水解反应的是( )?
| A、蛋白质 | B、油脂 |
| C、蔗糖 | D、葡萄糖 |
下列能通过化合反应制取的物质是( )
①Fe(OH)3 ②FeCl2 ③Fe(NO3)2 ④FeI2.
①Fe(OH)3 ②FeCl2 ③Fe(NO3)2 ④FeI2.
| A、①② | B、②③④ |
| C、①②③ | D、①②③④ |
下列叙述正确的是( )
| A、鸡蛋白溶液中,加入浓的硫酸铵溶液有沉淀析出,加入水后沉淀不溶解 |
| B、蛋白质水解的最后产物是氨基酸 |
| C、重金属盐使蛋白质变性,所以吞食“钡餐”会引起中毒 |
| D、人体中的氨基酸都不能自身合成 |
用NA代表阿伏加德罗常数的值,如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是( )L.
A、
| ||
B、
| ||
C、
| ||
D、
|
某溶液中含有CH3COO-、SO
、SO
、HCO
、CO
五种离子,将过量的Na2O2固体加入其中后,仍能大量存在的离子是( )
2- 4 |
2- 3 |
- 3 |
2- 3 |
A、CH3COO-、SO
| ||||||
B、SO
| ||||||
C、SO
| ||||||
D、CH3COO-、SO
|
 在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )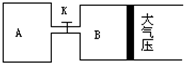 如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答: