题目内容
将Na2CO3?10H2O和NaHCO3的混合物11.94g,溶于水配制成200mL溶液,测得Na+浓度c(Na+)=0.5mol/L.若将11.94g该混合物加热至质量不再改变时,得到的固体物质的质量为( )
| A、3.1g | B、5.3g |
| C、9.0g | D、11.0g |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:Na2CO3?10H2O和 NaHCO3的混合物加热分解,最终固体物质为Na2CO3,根据钠离子守恒,可知n(Na2CO3)=
n(Na+),根据n=cV计算混合物中含有的n(Na+),再根据m=nM计算最终得到的固体碳酸钠的质量.
| 1 |
| 2 |
解答:
解:混合物中含有的n(Na+)=0.2L×0.5mol/L=0.1mol,
Na2CO3?10H2O和 NaHCO3的混合物加热分解,最终固体物质为Na2CO3,根据钠离子守恒,可知n(Na2CO3)=
n(Na+)=0.1mol×
=0.05mol,最终得到的固体碳酸钠的质量为0.05mol×106g/mol=5.3g,
故选:B.
Na2CO3?10H2O和 NaHCO3的混合物加热分解,最终固体物质为Na2CO3,根据钠离子守恒,可知n(Na2CO3)=
| 1 |
| 2 |
| 1 |
| 2 |
故选:B.
点评:本题考查混合物的有关计算,难度中等,注意利用钠离子守恒进行的计算,侧重对学生思维能力的考查.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
某有机物6g与足量钠反应,生成0.05mol氢气,该有机物可能是( )
| A、CH3CH2OH |
B、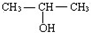 |
| C、CH3OH |
| D、CH3-O-CH2CH3 |
在铝热反应中,铝粉的作用是( )
| A、还原剂 | B、催化剂 |
| C、氧化剂 | D、既是氧化剂又是氧化剂 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4 L 苯中含有NA个苯分子 |
| B、1 mol/L NaCl溶液含有NA个Na+ |
| C、1 mol Fe和足量稀硝酸反应产生22.4LNO |
| D、16 g CH4中含有4 NA个C-H键 |
能检验淀粉是否完全水解的试剂是( )
| A、溴水 | B、碘水 |
| C、碘化钾 | D、银氨溶液 |
下列各组离子在溶液中可以大量共存的是( )
| A、H+、SO32-、S2-、K+ |
| B、Na+、K+、S2-、SO42- |
| C、HSO3-、Cl-、OH-、Ba2+ |
| D、Cu2+、Cl-、OH-、K+ |
下列叙述不正确的是( )
①工业上用电解氯化钠溶液的方法制取钠
②可以用钠加入氯化镁的饱和溶液中制取金属镁
③用于电冶铝的原料是氯化铝
④炭在高温下能还原氧化镁中的镁.
①工业上用电解氯化钠溶液的方法制取钠
②可以用钠加入氯化镁的饱和溶液中制取金属镁
③用于电冶铝的原料是氯化铝
④炭在高温下能还原氧化镁中的镁.
| A、①②③④ | B、①②③ |
| C、①③ | D、① |
下列物质中,不跟烧碱溶液反应的是( )
| A、二氧化硅 | B、二氧化碳 |
| C、硅 | D、石墨 |