题目内容
16.设NA表示阿伏伽德罗常数的数值,下列说法正确的是( )| A. | 1mol H3O+中含有的电子数目为11NA | |
| B. | 5.8g熟石膏(2CaSO4•H2O)含有的结晶水分子数目为0.04NA | |
| C. | 28g聚乙烯含有的碳原子数目为2NA | |
| D. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1 mol•L-1 |
分析 A.1个H3O+中含有11个电子,根据N=nNA计算电子数目;
B.依据公式n=$\frac{m}{M}$将质量换算成物质的量,结合2CaSO4•H2O化学式计算;
C.聚乙烯最简式为CH2,据此解答;
D.溶液的体积不等于水的体积.
解答 解:A.1个H3O+中含有11个电子,故1molH3O+中含有11mol电子,N=nNA=11NA,故A正确;
B.1mol2CaSO4•H2O含有结晶水1mol,5.8g 2CaSO4•H2O物质的量=$\frac{5.8g}{290g/mol}$=0.02mol,则含有的结晶水分子数为0.02NA,故B错误;
C.28 g聚乙烯含有CH2物质的量为:$\frac{28g}{14g/mol}$=2mol,含有的碳原子数为2NA,故C正确;
D.溶液的体积不等于水的体积,所以含NA个Na+的Na2O溶解于1L水中形成溶液的体积不知道,无法计算其浓度,故D错误;
故选AC.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大,注意可以把聚乙烯看成CH2.

练习册系列答案
相关题目
16.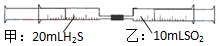 常温下,将甲针筒内20mLH2S推入含有10mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )
常温下,将甲针筒内20mLH2S推入含有10mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )
 常温下,将甲针筒内20mLH2S推入含有10mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )
常温下,将甲针筒内20mLH2S推入含有10mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )| A. | 有淡黄色固体生成 | B. | 有无色液体生成 | ||
| C. | 气体体积缩小 | D. | 最终约余15mL气体 |
4.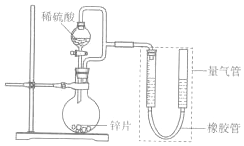 某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
(1)用上述装置探究影响化学反应速率的因素.以生成9.0mL气体为计时终点,结果为t1>t2.
①比较实验I和Ⅱ可以得出的实验结论是在其他条件一定时,化学反应速率随反应物浓度的增大而增大.
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据.粗锌片中所含杂质可能是BCD (填序号).
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀
①圆底烧瓶中的试剂可选用BD(填序号)
A.稀HCl B.NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是量气管右端液面下降,左端液面上升.
 某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:(1)用上述装置探究影响化学反应速率的因素.以生成9.0mL气体为计时终点,结果为t1>t2.
| 序号 | V(H2SO4)/mL | C(H2SO4)/mol•L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据.粗锌片中所含杂质可能是BCD (填序号).
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀
①圆底烧瓶中的试剂可选用BD(填序号)
A.稀HCl B.NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是量气管右端液面下降,左端液面上升.
11.可用来鉴别乙醇、乙醛的试剂是( )
| A. | 银氨溶液 | B. | 乙酸溶液 | C. | 氯化铁溶液 | D. | 氢氧化钠溶液 |
1.化学与生活、社会密切相关,下列有关说法中不正确的是( )
| A. | 用NaHCO3和Al2(SO4)3溶液可以制作泡沫灭火剂 | |
| B. | 为了防止蛋白质盐析,疫苗等生物制剂应冷冻保藏 | |
| C. | 溴化银见光易分解,可用作胶片感光剂 | |
| D. | 硅胶多孔,常用作食品干燥剂 |
8.生活中下列物质起还原作用的是( )
| A. | 明矾作净水剂 | B. | 硅胶作干燥剂 | C. | 铁粉作脱氧剂 | D. | 活性炭作吸附剂 |
5.同主族元素形成的同一类型化合物,往往其结构和性质相似.PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是( )
| A. | 它是一种共价化合物 | |
| B. | 它只含共价键 | |
| C. | 它不可能与NaOH溶液反应 | |
| D. | 它受热时,可能会分解产生有色气体 |
6.设NA为阿伏加徳罗常数值.下列有关叙述正确的是( )
| A. | 2 molSO2与3 molO2反应生成的SO3分子数为2NA | |
| B. | 30 g乙酸和葡萄糖混合物中的氢原子数为2NA | |
| C. | 常温下pH=12的NaOH溶液中,水电离出的氢离子数为10-12NA | |
| D. | 标准状况下,2.24 L C2H6含有的共价键数为0.6NA |