题目内容
11.把铝粉与Fe3O4的混合物,分为两等份.前一份在高温下恰好完全反应,之后将生成物与足量盐酸充分反应;后一份直接加入足量NaOH溶液充分反应.前后两种情况下生成的气体在同温同压下的体积比是( )| A. | 1:1 | B. | 3:4 | C. | 9:8 | D. | 4:3 |
分析 把Fe3O4和铝粉配成铝热剂,分成两等份,一份在高温下恰好完全反应生成铁与氧化铝,由电子转移守恒可知$\frac{8}{3}$n(Fe)=3n(Al),然后将生成物与足量的稀盐酸反应,铁与盐酸反应生成氯化亚铁与氢气,由电子转移守恒可知n(H2)=n(Fe);令一份直接加入足量的NaOH溶液使之充分反应,铝与氢氧化钠反应生成偏铝酸钠与氢气,由电子转移守恒可知2n′(H2)=3n(Al),据此计算判断.
解答 解:把Fe3O4和铝粉配成铝热剂,分成两等份,一份在高温下恰好完全反应生成铁与氧化铝,由电子转移守恒可知$\frac{8}{3}$n(Fe)=3n(Al),然后将生成物与足量的稀盐酸反应,铁与盐酸反应生成氯化亚铁与氢气,由电子转移守恒可知n(H2)=n(Fe),所以n(H2)=$\frac{9}{8}$n(Al);
令一份直接加入足量的NaOH溶液使之充分反应,铝与氢氧化钠反应生成偏铝酸钠与氢气,由电子转移守恒可知2n′(H2)=3n(Al),所以n′(H2)=$\frac{3}{2}$n(Al).
故两种情况下生成气体的物质的量之比为n(H2):n′(H2)=$\frac{9}{8}$n(Al):$\frac{3}{2}$n(Al)=3:4,故选:B.
点评 本题考查混合物的计算、根据方程式的计算,难度中等,本题采取电子转移守恒计算,比根据方程式简单容易,清楚反应过程是关键,注意混合物的计算中守恒的运用.

练习册系列答案
相关题目
1.如表是元素周期表的一部分,针对表中元素,填写下列空白.
(1)Al3+的结构示意图为 .
.
(2)CO2中存在的化学键是共价键,CO2的电子式为 .
.
(3)上述元素中,金属性最强的元素是Na(填元素符号,下同),原子半径最小的元素是F.
(4)F、Cl、S的氢化物中稳定性最弱的是H2S(填化学式,下同).N、P、Si的最高价氧化物对应水化物中酸性最强的是HNO3.
(5)Na、Al最高价氧化物的水化物之间反应的化学方程式是NaOH+Al(OH)3=NaAlO2+2H2O.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | Li | Be | B | C | N | O | F |
| 3 | Na | Mg | Al | Si | P | S | Cl |
 .
.(2)CO2中存在的化学键是共价键,CO2的电子式为
 .
.(3)上述元素中,金属性最强的元素是Na(填元素符号,下同),原子半径最小的元素是F.
(4)F、Cl、S的氢化物中稳定性最弱的是H2S(填化学式,下同).N、P、Si的最高价氧化物对应水化物中酸性最强的是HNO3.
(5)Na、Al最高价氧化物的水化物之间反应的化学方程式是NaOH+Al(OH)3=NaAlO2+2H2O.
2.热化学方程式C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol表示( )
| A. | 碳和水反应吸收131.3kJ 能量 | |
| B. | 1mol 碳和1mol 水反应生成一氧化碳和氢气并吸收131.3kJ 热量 | |
| C. | 1mol 固态碳和1mol 水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ | |
| D. | 1 个固态碳原子和1 分子水蒸气反应吸热131.1kJ |
16.一定量碳(由12C、13C组成)和足量氧气(由16O组成)反应所得CO2气体,对氢气的相对密度为22.495,则该碳中12C和13C的原子个数比为( )
| A. | 1:99 | B. | 1:100 | C. | 100:1 | D. | 99:1 |
3.下列关于水的叙述错误的是( )
| A. | 自然界中的水都是混合物 | B. | 工业废水可直接排放 | ||
| C. | 水是生命活动不可缺少的物质 | D. | 肥皂水可以区分软水和硬水 |
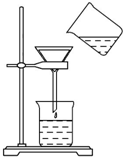 将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:
将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题: $→_{△}^{氧化/催化剂}$
$→_{△}^{氧化/催化剂}$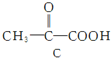 $→_{△}^{H_{2}/Ni}$
$→_{△}^{H_{2}/Ni}$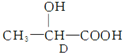
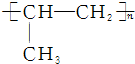 .
. .
.