��Ŀ����
19��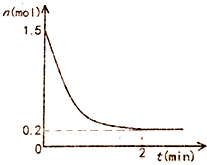 ��һ����̶�Ϊ10L���ܱպ��������г���1.5mol������������Ӧ��2NH3��g��?N2��g��+3H2��g����H=93KJ/mol��Ӧ������NH3���ʵ�����ʱ��ı仯��ͼ��ʾ��
��һ����̶�Ϊ10L���ܱպ��������г���1.5mol������������Ӧ��2NH3��g��?N2��g��+3H2��g����H=93KJ/mol��Ӧ������NH3���ʵ�����ʱ��ı仯��ͼ��ʾ����1��2minʱ��Ӧ���뻯ѧƽ��״̬����ʱ����������Ũ��c��H2��=0.195mol/L��
��2��0��2min����NH3��ʾ��ƽ����Ӧ����v��NH3��=0.065mol/��L•min����
��3����ͼ�������жϡ�0��2min��NH3�ֽⷴӦ���ȿ��������ȿ��������������족�����ٽ��С�����
��4����������ʼʱ��ƽ��ʱ��ѹǿ��Ϊ15��28��
���� ��1����ͼ��֪��NH3���ʵ�������1.5mol-0.2mol=1.3mol����Ϸ�Ӧ��֪��������Ϊ1.3mol��$\frac{3}{2}$=1.95mol�����c=$\frac{n}{V}$���㣻
��2�����v=$\frac{��c}{��t}$���㣻
��3����ʼŨ�ȴ�Ӧ���ʿ죬����Ũ�ȼ�С���ҷ�ӦΪ���ȷ�Ӧ���¶Ƚ��ͣ�
��4��2NH3��g��?N2��g��+3H2��g��
��ʼ 1.5 0 0
ת�� 1.3 0.65 1.95
ƽ�� 0.2 0.65 1.95
���ѹǿ֮�ȵ������ʵ���֮�ȼ��㣮
��� �⣺��1����ͼ��֪��NH3���ʵ�������1.5mol-0.2mol=1.3mol����Ϸ�Ӧ��֪��������Ϊ1.3mol��$\frac{3}{2}$=1.95mol�����ʱ����������Ũ��c��H2��=$\frac{1.95mol}{10L}$=0.195mol/L���ʴ�Ϊ��0.195��
��2��0��2min����NH3��ʾ��ƽ����Ӧ����v��NH3��=$\frac{\frac{1.3mol}{10L}}{2min}$=0.065mol/��L•min�����ʴ�Ϊ��0.065��
��3����ʼŨ�ȴ�Ӧ���ʿ죬����Ũ�ȼ�С���ҷ�ӦΪ���ȷ�Ӧ���¶Ƚ��ͣ���ֽ������ȿ�������ʴ�Ϊ���ȿ������
��4��2NH3��g��?N2��g��+3H2��g��
��ʼ 1.5 0 0
ת�� 1.3 0.65 1.95
ƽ�� 0.2 0.65 1.95
��ѹǿ֮�ȵ������ʵ���֮�ȿ�֪����������ʼʱ��ƽ��ʱ��ѹǿ��Ϊ$\frac{1.5}{0.2+0.65+1.95}$=15��28��
�ʴ�Ϊ��15��28��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����ͼ�����ʵ����仯�����ʼ�ѹǿ�ȵļ���Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ͼ���Ӧ�ã���Ŀ�ѶȲ���

| A�� | NaOH�TNa++O2-+H+ | B�� | MgCl2�TMg2++Cl22- | ||
| C�� | KClO3�TK++Cl-+3O2- | D�� | NH4NO3�TNH4++NO3- |
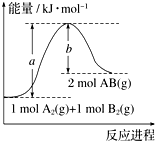 ͼ�����о���ѧ��Ӧ���ʱ��һ�ֳ��÷�������֪��ѧ��ӦA2��g��+B2��g���T2AB��g���������仯������ͼ��ʾ����������������ȷ���ǣ�������
ͼ�����о���ѧ��Ӧ���ʱ��һ�ֳ��÷�������֪��ѧ��ӦA2��g��+B2��g���T2AB��g���������仯������ͼ��ʾ����������������ȷ���ǣ�������| A�� | ÿ����2 mol ABʱ���գ�a-b�� kJ���� | |
| B�� | �÷�Ӧ�ȡ�H=+��a-b�� kJ•mol-1 | |
| C�� | �÷�Ӧ�з�Ӧ�������������������������� | |
| D�� | ����1 mol A-A��1 mol B-B��ʱ�ų�a kJ���� |
| �¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| A�� | 4 sʱc��B��Ϊ0.38 mol/L | |
| B�� | 830���ƽ��ʱ��A��ת����Ϊ80% | |
| C�� | ��Ӧ��ƽ��������¶ȣ�ƽ�������ƶ� | |
| D�� | 1200��ʱ��ӦC��g��+D��g��?A��g��+B��g����ƽ�ⳣ����ֵΪ2.5 |