��Ŀ����
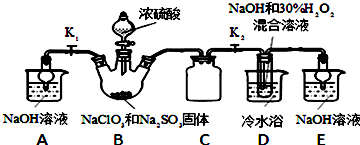
10��ij����С��̽�����÷ϺϽ𣨺�����������ͭ����ĩ��ȡ�������Ȼ�����Һ���̷�����͵������壬��ʵ�鷽����ͼ��
�Իش��������⣺
��1�������ٵ�����Ϊ���ˣ����õIJ����������ձ�������������©����
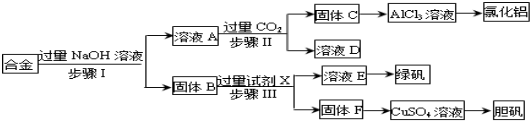
��2��д��A��D��Ӧ���ӷ���ʽAlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
��3����ҺE������Ũ������ȴ�ᾧ���̷����壮
��4��������F��CuSO4��Һ��;��I��;�������֣�����Ϊ���;����;����������;���������������࣬�Ҳ�������������Ⱦ������
��5��һ���¶��£�ijͬѧ���̷����Լ0.1mol•L-1FeSO4��Һ�������Һ��pH=3���������ӷ���ʽ����ԭ��Fe2++2H2O?Fe��OH��2+2H+������Һ��c��SO${\;}_{4}^{2-}$��-c��Fe2+��=5��10-4mol•L-1������ֵ����
��6����Ҫ�ⶨ������Һ��Fe2+��ȷŨ�ȣ�ȡ20.00mL��Һ����ƿ�У�����ֱ��������b�����ţ�����Һ���еζ���
a��0.1mol•L-1NaOH��Һ b��0.02•L-1KMnO4������Һ
c��0.20mol•L-1KMnO4������Һ d��0.10mol•L-1KSCN��Һ
�ζ��յ�������ǵ������һ��0.02 mol•L-1 KMnO4������Һ����Һ����ɫ��Ϊdz��ɫ����dz�Ϻ�ɫ������30s�ڲ���ɫ��
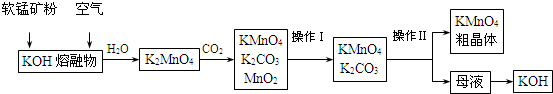
���� �ϺϽ𣨺�����������ͭ����ĩ�м��������ռ���Һ��ֻ�������䷴Ӧ���ܽ⣬���˺������B�ijɷ�Ϊ����ͭ����ҺAΪƫ��������Һ����ҺA��ͨ������Ķ�����̼���壬��������������������B�м���ϡ���ᣬ���˵���ҺEΪ���ữ������Һ��������������Һ������Ũ������ȴ�ᾧ���̷����壬Ȼ���پ����ˡ��þƾ�ϴ�ӡ����T�ó�Ʒ���þƾ�ϴ�ӿ��Լ��������������ܽ����ʧ��ͬʱ���������FΪͭ��;����Ϊͭ��������Ũ������������ͭ��ͬʱ�����ɶ����������壬;����Ϊͭ��������Ӧ��������ͭ������ͭ��ϡ���ᷴӦ��������ͭ������;���������������ʸ���û����Ⱦ���ݴ˴��⣮
��� �⣺��1�������ٵ�����Ϊ���ˣ����õ�����������̨����Ȧ���ձ�������Ҫ����Ʒ��©��������������ֽ��
�ʴ�Ϊ�����ˣ�©����
��2��A��DΪƫ��������Һ������Ķ�����̼��Ӧ��������������̼�����ƣ���Ӧ�����ӷ���ʽΪAlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�ʴ�Ϊ��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
��3������������Һ������Ũ������ȴ�ᾧ���̷����壬Ȼ���پ����ˡ�ϴ�ӡ����T�ó�Ʒ��
�ʴ�Ϊ����ȴ�ᾧ��
��4�������������֪��������F��CuSO4��Һ�����;������Ϊ;���������������࣬�Ҳ�������������Ⱦ������
�ʴ�Ϊ��;����;���������������࣬�Ҳ�������������Ⱦ������
��5��FeSO4��Һ�У���������ˮ��ʹ��Һ�����ԣ���Ӧ�����ӷ���ʽΪFe2++2H2O?Fe��OH��2+2H+�����ݵ���غ���2c��SO42-��-2c��Fe2+��=c��H+��-c��OH-��=1��10-3�����ԣ�SO42-��-c��Fe2+��=5��10-4��
�ʴ�Ϊ��Fe2++2H2O?Fe��OH��2+2H+��5��10-4��
��6��Ҫ�ⶨ������Һ��Fe2+��ȷŨ�ȣ����������Ը��������Һ�ζ���ѡ�������Ը��������Һʱ����Һ��Ũ���ʵ�ϡһ��Ϻã������ζ���ȷ�Ƚϸߣ�����ѡb���ζ��յ�������ǵ������һ��0.02 mol•L-1 KMnO4������Һ����Һ����ɫ��Ϊdz��ɫ����dz�Ϻ�ɫ������30s�ڲ���ɫ��
�ʴ�Ϊ��b�� �������һ��0.02 mol•L-1 KMnO4������Һ����Һ����ɫ��Ϊdz��ɫ����dz�Ϻ�ɫ������30s�ڲ���ɫ��
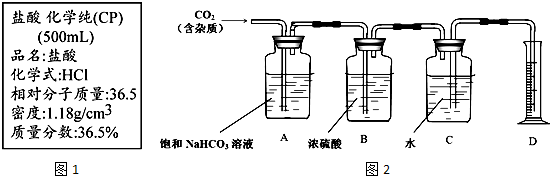
���� ������Ҫ�����˴ӹ�ҵ��������ȡ�����ע��ӿ�ͼת�����ҳ�������Ϣ�������йصĻ�ѧ��Ӧ���н���Ѷ��еȣ�

 ��У����ϵ�д�
��У����ϵ�д�| A�� | ���ʵ��� | B�� | Ħ������ | C�� | �������� | D�� | ���ʵ���Ũ�� |
| ���ܵ���� | Mg��OH��2 | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| �ܽ��/g | 9��10-4 | 1.7��10-6 | 1.5��10-4 | 3.0��10-9 |
��Ϊ�˳�ȥ�Ȼ���е�����Fe3+���Ƚ����������ˮ���ټ���һ�������Լ���Ӧ�����˽ᾧ���ɣ�
��Ϊ�˳�ȥ�Ȼ�þ�����е�����Fe3+���Ƚ����������ˮ������������������þ����ַ�Ӧ�����˽ᾧ���ɣ�
��Ϊ�˳�ȥ����ͭ�����е�����Fe2+���Ƚ����������ˮ������һ������H2O2����Fe2+������Fe3+��������Һ��pH=4�����˽ᾧ���ɣ�
��ش��������⣺
��1���������ֳ��ӷ������ܹ��ﵽ�ܺõ�Ч����Fe3+��Fe2+����ת��ΪFe��OH��3���ѧʽ������ȥ��
��2�����м�����Լ�Ӧ��ѡ��ˮΪ�ˣ���ԭ���Dz��������µ����ʣ�
��3�����г�ȥFe3+�����������ӷ���ʽΪ2Fe3+��aq��+3Mg��OH��2��s���T3Mg2+��aq��+2Fe��OH��3��s����
��4�������뷽������ص������У���ȷ����ACDE��
A��H2O2����ɫ�������������������в��������ʣ���������Ⱦ
B����Fe2+����ΪFe3+����Ҫԭ����Fe��OH��2������Fe��OH��3�������ѹ���
C��������ҺpH=4��ѡ����Լ���������ͭ���ʽ̼��ͭ
D��Cu2+���Դ���������pH=4����Һ��
E����pH��4����Һ��Fe3+һ�����ܴ������ڣ�
| A�� | ������Һ������������Һ��Ӧ�����ӷ���ʽΪH++OH-=H2O | |
| B�� | H2S��ˮ��Һ�еĵ��룺H2S+H2O?H3O++HS- | |
| C�� | �����ȼ����Ϊ890.3 kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O ��g����H=-890.3 kJ•mol-1 | |
| D�� | ˫��ˮ�м���ϡ�����KI��Һ��H2O2+2I-+H+�TI2+2H2O |

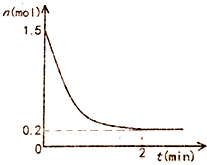 ��һ����̶�Ϊ10L���ܱպ��������г���1.5mol������������Ӧ��2NH3��g��?N2��g��+3H2��g����H=93KJ/mol��Ӧ������NH3���ʵ�����ʱ��ı仯��ͼ��ʾ��
��һ����̶�Ϊ10L���ܱպ��������г���1.5mol������������Ӧ��2NH3��g��?N2��g��+3H2��g����H=93KJ/mol��Ӧ������NH3���ʵ�����ʱ��ı仯��ͼ��ʾ��