题目内容
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应: KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:___________________
(2)该反应中还原剂和氧化剂的物质的量之比为______________;
(3)如果反应中转移1mol电子,则生成I2的物质的量为____________;
【答案】 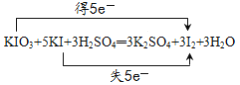 5:1 0.6mol
5:1 0.6mol
【解析】(1)反应物KIO3中I元素化合价为+5价,KI中I元素化合价为-1价,反应中I元素化合价分别由+5价、-1价变化为0价,可知(KIO3):n(KI)=1:5,结合质量守恒配平方程式为KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O,电子转移的方向与数目用双线桥法表示为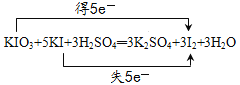 ,故答案为:
,故答案为: ;
;
(2)KIO3为氧化剂,KI为还原剂,由方程式可知,还原剂和氧化剂的物质的量之比为5:1,故答案为:5:1;
(3)在上述反应中,转移5mol电子生成碘单质的量是3mol,所以如果反应中转移1mol电子,则生成I2的物质的量为0.6moL,故答案为:0.6mol。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

