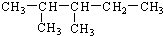题目内容
7.下面有关晶体的叙述中,正确的是( )| A. | 金刚石为网状结构,由共价键形成的碳原子环中,最小的环上有4个碳原子 | |
| B. | 12 g石墨中含有4NA个C-C键 | |
| C. | 氯化铯晶体中,每个Cs+周围紧邻8个Cl- | |
| D. | 干冰晶体中,每个CO2分子周围紧邻6个CO2分子 |
分析 A.金刚石的结构中,每个碳原子能形成4个共价键,根据教材图片确定由共价键形成的最小碳环上的碳原子个数;
B.在石墨晶体中1个C原子对应3×0.5=1.5个C-C键.C.氯化铯晶体晶胞结构如图: ,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点;D.采用沿X、Y、Z三轴切割的方法判断二氧化碳分子的个数.
,Cs+位于该晶胞的体心;而Cl-位于该晶胞的顶点;D.采用沿X、Y、Z三轴切割的方法判断二氧化碳分子的个数.
解答 解:A.根据教材图片知,金刚石结构中,每个碳原子能形成4个共价键,由共价键形成的最小碳环上有6个碳原子,故A错误;
B.在石墨晶体中1个C原子对应1.5个C-C键,12 g石墨中含有C-C键的个数为1.5NA,故B错误.C.根据晶胞图片知,在CsCl晶体中每个Cs+周围都紧邻8个Cl-,每个Cs+等距离紧邻的有6个Cs+,故C正确;D.根据教材图片,采用沿X、Y、Z三轴切割的方法判断二氧化碳分子的个数为12,所以在CO2晶体中,与每个CO2分子周围紧邻的有12个CO2分子;故D错误,故选C.
点评 本题考查晶体结构,明确晶胞结构是解本题关键,难点是配位数的计算,题目难度中等.

练习册系列答案
相关题目
17.下列二者之间是同分异构体关系的是( )
| A. | 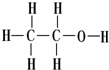 和 和 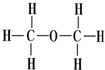 | B. | 金刚石和石墨 | C. | 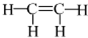 和H-C≡C-H 和H-C≡C-H | D. | O3和O2 |
18.粗盐中含有不溶性泥沙,可溶性的CaCl2、MgCl2以及一些硫酸盐等.精制食盐水的实验操作顺序如下:①加入过量BaCl2溶液,②加入过量NaOH溶液,③加入过量Na2CO3溶液,④过滤,⑤加入适量盐酸.下列说法不正确的是( )
| A. | ①②③中加入过量的试剂是为了完全除去相应的杂质离子 | |
| B. | ③中加入过量Na2CO3溶液仅为了完全除去Ca2+ | |
| C. | 因为Mg(OH)2难溶而MgCO3微溶,所以用NaOH除Mg2+效果比用Na2CO3好 | |
| D. | ⑤中可以通过边滴加边测定溶液pH的方法,控制加入的盐酸“适量” |
15.下列关于卤素的叙述说法错误的是( )
| A. | 单质的颜色随核电荷数的增加逐渐加深 | |
| B. | 元素的最高化合价均为+7 | |
| C. | 从上到下原子半径递增 | |
| D. | 从上到下非金属性减弱 |
2.化学家们合成了如图所示的一系列星烷,如三星烷、四星烷、五星烷等.下列说法不正确的是( )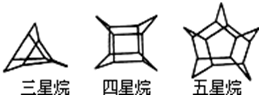

| A. | 三星烷与丙苯互为同分异构体 | B. | 五星烷的二氯取代物有8种 | ||
| C. | 六星烷的化学式为C18H24 | D. | 七星烷的一硝基取代物有2种 |
19.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| B. | 1.4g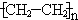 中含有的碳原子数为0.2NA 中含有的碳原子数为0.2NA | |
| C. | 1 mol苯分子中含有C=C双键数为3NA | |
| D. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA |
16.常温下,某无色透明的溶液中,下列各组离子能够大量共存的是( )
| A. | H+、Na+、Cl-、HCO3- | B. | Ba2+、Na+、SO42-、Cl- | ||
| C. | MnO4-、K+、S2-、H+ | D. | Mg2+、Cl-、NO${\;}_{3}^{-}$、H+ |