题目内容
10.四种短周期X、Y、Z、W在元素周期表中的位置如图所示.已知X、Y、Z三种元素的原子最外层电子数之和为15.下列说法正确的是( )| X | Z | |
| Y | W |
| A. | X是第ⅢA元素,Z是第ⅤA元素 | |
| B. | 原子半径大小关系:r(Y)<r(W) | |
| C. | Y的气态氢化物比Z的气态氢化物稳定 | |
| D. | X、Y、W三种元素的最高化合价依次升高 |
分析 X、Y、Z三种元素的原子最外层电子数之和为15,由元素在周期表中的位置可知X为C,Y为P,Z为O元素,则W为Cl元素,结合对应单质、化合物的性质以及元素周期率知识解答该题.
解答 解:A.由以上分析可知X为ⅣA族,Z为ⅥA族元素,故A错误;
B.同周期元素从左到右原子半径逐渐减小,则r(Y)>r(W),故B错误;
C.非金属性O>P,元素的非金属性越强,对应的氢化物越稳定,故C错误;
D.X、Y、W三种元素的最高化合价分别为+4、+5、+6,依次升高,故D正确.
故选D.
点评 本题考查了位置结构性质的相互关系及应用,为高考常见题型,侧重于学生的分析能力的考查,熟悉元素周期表结构及原子结构是解本题关键,结合元素周期律来分析解答,注意把握元素的性质与元素周期表的关系,难度不大.

练习册系列答案
相关题目
1.化学与生活密切相关,下列说法正确的是( )
| A. | 用热的烧碱溶液除去瓷器表面污垢 | |
| B. | 铝制餐具不宜长时间存放酸性、碱性或咸的物质 | |
| C. | 漂白粉长期放置空气中会被空气中的氧气氧化而变质 | |
| D. | 汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的 |
18.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在强碱性溶液中:Na+、K+、Al3+、Cl- | |
| B. | pH=1的溶液中:HCO3-、NH4+、NO3-、Ca2+ | |
| C. | 无色溶液中:Cu2+、NO3-、Cl-、H+ | |
| D. | 无色溶液中:Na+、K+、ClO-、SO42- |
5.下列离子方程式书写错误的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+6H2O+2OH-═2 Al(OH)4-+H2↑ | |
| B. | Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-═Al(OH)4- | |
| C. | NaAl(OH)4溶液中通入足量的CO2:2 Al(OH)4-+CO2═2Al(OH)3↓+CO32-+H2O | |
| D. | Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-═2 Al(OH)4-+H2O |
2.自来水可以用氯气消毒,某学生用这种自来水配制下列物质溶液,不会产生明显的药品变质的是( )
| A. | AgNO3 | B. | NaOH | C. | Na2CO3 | D. | AlCl3 |
19.X、Y、Z、W 是短周期元素,其在周期表的位置如图,请找出错误选项( )
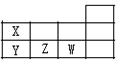

| A. | 原子半径:Y>Z>W | B. | 酸性:HWO4>HXO3>H3YO4 | ||
| C. | 热稳定性:HW>XH3>YH3 | D. | 离子半径:Y3-<Z2-<W- |
20.下列化学用语正确的是( )
| A. | HCl的电子式 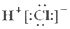 | B. | Cl-的结构示意图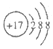 | ||
| C. | CO2的电子式 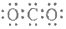 | D. | 质量数为37的氯原子 ${\;}_{37}^{17}$Cl |