题目内容
 电化学在工业生产中有广泛应用.如图所示,水槽中试管内有一枚铁钉,放置数天观察,发现铁钉被腐蚀.
电化学在工业生产中有广泛应用.如图所示,水槽中试管内有一枚铁钉,放置数天观察,发现铁钉被腐蚀.(1)若试管内液面上升,发生
负极:
(2)若试管内液面下降,则烧杯中的溶液呈
考点:探究铁的吸氧腐蚀
专题:
分析:(1)若试管内液面上升,说明试管内气体压强减小,则铁钉发生吸氧腐蚀,碱性或中性条件下,铁钉发生吸氧腐蚀,负极上铁失电子,正极上氧气得电子;
(2)若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,正极上氢离子得电子发生还原反应,电极反应式为4H++4e-═2H2↑.
(2)若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,正极上氢离子得电子发生还原反应,电极反应式为4H++4e-═2H2↑.
解答:
解:(1)若试管内液面上升,说明试管内气体压强减小,则铁钉发生吸氧腐蚀,碱性或中性条件下,铁钉发生吸氧腐蚀,负极上铁失电子,电极反应式为Fe-2e-═Fe2+,正极上氧气得电子,电极反应式为2H2O+O2+4e-═4OH-,
故答案为:吸氧;Fe-2e-═Fe2+;2H2O+O2+4e-═4OH-;
(2)若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-═Fe2+,正极上氢离子得电子发生还原反应,
故答案为:酸;2H++2e-═H2↑.
故答案为:吸氧;Fe-2e-═Fe2+;2H2O+O2+4e-═4OH-;
(2)若试管内液面下降,说明试管内气体压强增大,则铁钉发生析氢腐蚀,酸性条件下、铁钉发生析氢腐蚀,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-═Fe2+,正极上氢离子得电子发生还原反应,
故答案为:酸;2H++2e-═H2↑.
点评:铁发生腐蚀类型可根据试管内液面的变化确定,再结合发生析氢腐蚀和吸氧腐蚀的条件来分析解答,难点是电极反应式的书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应中,属于非氧化还原反应的是( )
| A、3CuS+8HNO3═3Cu(NO3)2+2NO↑+3S↓+4H2O |
| B、3Cl2+6KOH═5KCl+KClO3+3H2O |
| C、Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O |
| D、CuCl2+Ba(OH)2═Cu(OH)3↓+BaCl2 |
已知元素R有某种核素的离子Rx+,该离子核内中子数为Y,核外电子数为Z,该核素的符号为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
常温下,下列各组离子一定能大量共存的是( )
| A、滴加石蕊显红色的溶液中:Na+、Fe2+、Cl-、NO3- | ||
B、
| ||
| C、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- | ||
| D、由水电离的c(H+)=1.0×10-13 mol?L-1的溶液中:K+、NH4+、AlO2-、HCO3- |

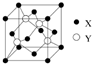 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1.元素Y基态原子的3p轨道上有5个电子.元素Z的原子最外层电子数是其内层的3倍.元素W基态原子的核外电子共有16种运动状态.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1.元素Y基态原子的3p轨道上有5个电子.元素Z的原子最外层电子数是其内层的3倍.元素W基态原子的核外电子共有16种运动状态.