题目内容
6.下列实验设计及其对应的离子方程式均正确的是( )| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| C. | 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
分析 A.铁离子与铜反应生成亚铁离子和铜离子;
B.2mol过氧化钠与水反应生成1mol氧气,该反应不满足电子守恒;
C.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
D.酸性高锰酸根离子能够氧化氯离子,干扰了检验结果.
解答 解:A.用FeCl3溶液腐蚀铜线路板,反应生成氯化亚铁和氯化铜,反应的离子方程式为:Cu+2Fe3+═Cu2++2Fe2+,故A正确;
B.Na2O2与H2O反应制备O2,正确的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故B错误;
C.将氯气溶于水制备次氯酸,次氯酸应该保留分子式,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故C错误;
D.酸性高锰酸钾能够氧化盐酸中的氯离子,无法证明H2O2具有还原性,应该用浓硝酸或浓硫酸酸化,故D错误;
故选A.
点评 本题考查了离子方程式的判断,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.已知有下列反应:4KI+2CuSO4=I2+Cu2I2↓(白色)+2K2SO4;I2+2S2O32-═S4O62-+2I-;Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O
(1)现要测定100.00mL硫酸铜溶液中铜离子的物质的量浓度,其测定过程如下:用移液管准确量取20,.00mL硫酸铜溶液于锥形瓶中,加入过量KI固体,充分反应,生成白色沉淀,用0,.1000mol/LNa2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液19.80mL.
①滴定过程应选用作指示剂淀粉,滴定终点的现象是最后一滴溶液滴下,溶液恰好由蓝色变为无色,且半分钟内不变化.
②下列有关该实验中的图示和操作都正确的是C.
A.图A表示用移液管移取A溶液到锥形瓶中的操作 B.图B表示对滴定管读数
C.图C表示排气泡操作 D.图D表示滴定操作

③溶液A中铜离子的物质的量浓度为0.099mol/L.
④下列实验操作会使得测定结果偏高的是B.
A.锥形瓶用蒸馏水洗涤后,直接盛待测液
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴无气泡
C.摇荡锥形瓶时溶液溅出
D.锥形瓶中溶液颜色发生变化时立即读数
(2)某实验兴趣小组为了研究外界条件对Na2S2O3与硫酸反应速率的影响,设计如下实验方案:
①判断上述反应速率快慢的实验现象是出现淡黄色沉淀的快慢.
②实验比较法是人们研究各类问题常用的方法,但在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰.上述A组和B组比较的是硫酸浓度的改变对反应速率的影响,则B组中加水的体积a=10mL.
③由A组和C组实验比较可以得出的结论是其他条件相同时,温度越高,反应速率越快.
(1)现要测定100.00mL硫酸铜溶液中铜离子的物质的量浓度,其测定过程如下:用移液管准确量取20,.00mL硫酸铜溶液于锥形瓶中,加入过量KI固体,充分反应,生成白色沉淀,用0,.1000mol/LNa2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液19.80mL.
①滴定过程应选用作指示剂淀粉,滴定终点的现象是最后一滴溶液滴下,溶液恰好由蓝色变为无色,且半分钟内不变化.
②下列有关该实验中的图示和操作都正确的是C.
A.图A表示用移液管移取A溶液到锥形瓶中的操作 B.图B表示对滴定管读数
C.图C表示排气泡操作 D.图D表示滴定操作

③溶液A中铜离子的物质的量浓度为0.099mol/L.
④下列实验操作会使得测定结果偏高的是B.
A.锥形瓶用蒸馏水洗涤后,直接盛待测液
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴无气泡
C.摇荡锥形瓶时溶液溅出
D.锥形瓶中溶液颜色发生变化时立即读数
(2)某实验兴趣小组为了研究外界条件对Na2S2O3与硫酸反应速率的影响,设计如下实验方案:
组号 | 反应温度 (℃) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/ml | c/mol•L-1 | V/ml | c/mol•L-1 | V/ml | ||
| A | 10 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | a |
| C | 30 | 5 | 0.1 | 10 | 0.1 | 5 |
②实验比较法是人们研究各类问题常用的方法,但在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰.上述A组和B组比较的是硫酸浓度的改变对反应速率的影响,则B组中加水的体积a=10mL.
③由A组和C组实验比较可以得出的结论是其他条件相同时,温度越高,反应速率越快.
1.某有机物的结构简式如图,关于该物质的叙述错误的是( )
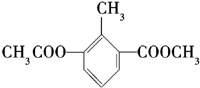

| A. | 一个分子中含有12个H原子 | B. | 苯环上的一氯代物有2种 | ||
| C. | 含有一种含氧官能团 | D. | 分子式是C11H12O4 |
11.下列说法不正确的是( )
| A. | 互为手性异构体的分子互为镜像 | |
| B. | 利用手性催化剂合成可主要得到一种手性分子 | |
| C. | 手性异构体分子组成相同 | |
| D. | 手性异构体性质相同 |
18.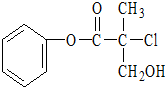 某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )
某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )
 某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )
某有机物A是农药生产中的一种中间体,其结构简式如图所示:下列关于A的叙述正确的是( )| A. | 属于卤代烃,易溶于水 | |
| B. | 在酸性或碱性条件下都能发生水解反应 | |
| C. | 1molA可以与2molNaOH反应 | |
| D. | 一定条件下可发生加成反应和消去反应 |
15.除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | 二氧化碳 | 一氧化碳 | 氢氧化钠溶液和浓硫酸 | 洗气 |
| B | 硫酸钡 | 碳酸钡 | 足量的稀硫酸 | 溶解、过滤、洗涤、烘干 |
| C | 氯化钙溶液 | 消石灰 | 过量的二氧化碳 | 过滤、蒸发、结晶 |
| D | 氨气 | 水 | 火碱溶液 | 通过盛有火碱溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
16.下列关于有机物性质的叙述错误的是( )
| A. | 甲烷和氯气在光照条件下反应产生油状液滴 | |
| B. | 乙烯能使溴的四氯化碳溶液褪色 | |
| C. | 苯能使酸性高锰酸钾溶液褪色 | |
| D. | 乙醇可以和金属钠反应放出氢气 |
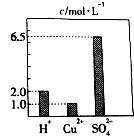 在0.2L由H2SO4、CuSO4和Al2(SO4)3组成的混合溶液中,部分离子浓度大小如图所示,请回答下列问题:
在0.2L由H2SO4、CuSO4和Al2(SO4)3组成的混合溶液中,部分离子浓度大小如图所示,请回答下列问题: