题目内容
已知:有如下四个化学反应2NaA+B2=2NaB+A2 2NaA+C2=2NaC+A2 2NaB+C2=2NaC+B2 2NaC+D2=2NaD+C2则氧化性由强到弱的顺序是( )
| A、A2>B2>C2>D2 |
| B、B2>A2>C2>D2 |
| C、C2>B2>A2>D2 |
| D、D2>C2>B2>A2 |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:根据氧化剂的氧化性强于氧化产物的氧化性判断;含有元素化合价降低的反应物为氧化剂,还原剂通过氧化反应生成的物质是氧化产物.
解答:
解:根据已知反应的离子方程式来判断如下:
①反应2NaA+B2=2NaB+A2 中B元素的化合价降低,B2是氧化剂,NaA发生氧化反应生成A2,A2是氧化产物,所以氧化性B2>A2;
②2NaA+C2=2NaC+A2 中C元素的化合价降低,C2是氧化剂,NaA发生氧化反应生成A2,A2是氧化产物,所以氧化性C2>A2;
③2NaB+C2=2NaC+B2中C元素的化合价降低,C2是氧化剂,NaB发生氧化反应生成B2,B2是氧化产物,所以氧化性C2>B2;
④2NaC+D2=2NaD+C2中D元素的化合价降低,D2是氧化剂,NaC发生氧化反应生成C2,C2是氧化产物,所以氧化性D2>C2;
所以氧化性为D2>C2>B2>A2.
故选D.
①反应2NaA+B2=2NaB+A2 中B元素的化合价降低,B2是氧化剂,NaA发生氧化反应生成A2,A2是氧化产物,所以氧化性B2>A2;
②2NaA+C2=2NaC+A2 中C元素的化合价降低,C2是氧化剂,NaA发生氧化反应生成A2,A2是氧化产物,所以氧化性C2>A2;
③2NaB+C2=2NaC+B2中C元素的化合价降低,C2是氧化剂,NaB发生氧化反应生成B2,B2是氧化产物,所以氧化性C2>B2;
④2NaC+D2=2NaD+C2中D元素的化合价降低,D2是氧化剂,NaC发生氧化反应生成C2,C2是氧化产物,所以氧化性D2>C2;
所以氧化性为D2>C2>B2>A2.
故选D.
点评:本题考查根据方程式来比较氧化性和还原性强弱,题目难度不大,解题的关键是根据化合价找出氧化剂、还原剂、氧化产物和还原产物.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
同分异构现象是造成有机物种类繁多的重要原因之一.下列物质不是1-戊烯(CH2=CH-CH2-CH2-CH3)的同分异构体的是( )
| A、CH3-CH=CH-CH2-CH3 |
B、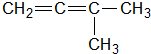 |
C、 |
D、 |
pH=3的盐酸与pH=3的NH4Cl溶液,其中由水电离出的H+浓度分别为C1和C2,则C1和C2大小关系是( )
| A、C1=C2 |
| B、8C1=C2 |
| C、C1=108C2 |
| D、C1=10-8C2 |
下列过程中△H小于零的是( )
| A、碳酸氢钠受热分解 |
| B、氯化铵分解得氨气 |
| C、碳酸钙分解得二氧化碳 |
| D、实验室制备氢气 |
下列化学反应中,属于氧化还原反应的是( )
| A、Na2CO3+BaCl 2═BaCO3↓+2NaCl | ||||
| B、2AgNO3+Cu═Cu(NO3)2+2Ag | ||||
C、2NaHCO3
| ||||
| D、Na2O+H2O═2NaOH |
铋(Bi)是氮族元素中原子序数最大的元素,试推测铋单质或其化合物可能具有的性质是( )
| A、铋能形成很稳定的气态氢化物 |
| B、铋的最高价氧化物对应的水化物的酸性比磷酸强 |
| C、铋单质可能具有良好的导电性并具有较大的密度 |
| D、铋的两种常见氧化物Bi2O3和Bi2O5,一定是碱性氧化物 |
用NA表示阿伏加德罗常数的数值,则下列说法中正确的是( )
| A、OH-的摩尔质量为17 g |
| B、标准状况下,22.4L水中含有的水分子数目为NA |
| C、24 g Mg变成Mg2+时转移电子的数目是NA |
| D、0.5 NA个Cl2的物质的量是0.5 mol |