题目内容
15.按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便.下列各组物质中,符合“氧化物-酸-碱-盐”顺序排列的是( )| A. | H2SO4 HCl Mg(OH)2 MgCl2 | B. | CO2 H2CO3 Na2CO3 Ca(HCO3)2 | ||
| C. | H2O HNO3 NaOH KNO3 | D. | SO3 NaHCO3 NaOH Na2SO4 |
分析 电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都是氢氧根离子的化合物是碱,由金属离子(或铵根离子)和酸根离子组成的化合物是盐.氧化物是由两种元素组成并且一种元素是氧元素的化合物.
解答 解:A、H2SO4属于酸,HCl属于酸,氢氧化镁属于碱,氯化镁是由金属离子和酸根离子组成的化合物,属于盐,故A错误;
B、二氧化碳属于氧化物,碳酸属于酸,Na2CO3 和Ca(HCO3)2属于盐,故B错误;
C、水属于氧化物,硝酸属于酸,氢氧化钠属于碱,硝酸钾属于盐,故C正确;
D、三氧化硫属于氧化物,碳酸氢钠属于盐,氢氧化钠属于碱,硫酸钠属于盐,故D错误.
故选C.
点评 本题考查酸、碱、盐以及氧化物的概念及分类,难度不大,注意把握概念,从电离的角度把握酸碱盐的实质以及识记物质的俗名.

练习册系列答案
相关题目
17.下列关于Na2CO3的说法中正确的是( )
| A. | Na2CO3溶液中c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) | |
| B. | Na2CO3溶液中滴加酚酞呈红色,加热红色变浅 | |
| C. | 0.1mol•L-1的Na2CO3溶液中c(Na+)>2c(CO32-) | |
| D. | 相同温度下,CaCO3在饱和Na2CO3溶液中的KSP比在纯水中的小 |
3.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 .
.
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”、“不变”).
②如表为反应在T1温度下的部分实验数据:
则500s内N2O5的分解速率为0.00296 mol•L-1•s-1.
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1(填>、<或=).
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2.
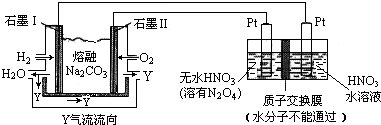
写出石墨Ⅰ电极上发生反应的电极反应式H2+CO32--2e-═H2O+CO2,N2O5在电解池的阳极区生成(填“阳极”或“阴极”).
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是
 .
.(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”、“不变”).
②如表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1(填>、<或=).
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2.

写出石墨Ⅰ电极上发生反应的电极反应式H2+CO32--2e-═H2O+CO2,N2O5在电解池的阳极区生成(填“阳极”或“阴极”).
10.下列关于能量变化的说法正确的是( )
| A. | “冰,水为之,而寒于水”说明相同质量的水和冰相比较,冰的能量高 | |
| B. | 化学反应必定同时遵循质量守恒和能量守恒 | |
| C. | 化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种 | |
| D. | 已知:C(石墨,s)═C(金刚石,s)△H>0,所以金刚石比石墨稳定 |
20.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温下,1 mol 铁放入足量的浓硫酸中转移的电子数为0 | |
| B. | 在标准状况下,4.48 L氧单质含有的氧原子数目为0.4NA | |
| C. | 在含有NA个CH3COO-的醋酸溶液中,H+数目略大于NA | |
| D. | 0.1 mol N5+ 微粒中含有的电子数为3.5NA |
7.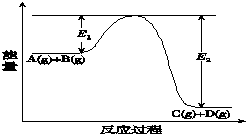 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
①图中E1代表的意义是反应物的活化能.
该反应是放热反应(填“吸热”或“放热”).反应热△H的表达式为E1-E2 .
②当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”).
(2)800℃时,在2L密闭容器内充入0.50mol NO和0.25mol O2,发生如下反应:2NO(g)+O2(g)═2NO2(g)△H<0.体系中,n(NO)随时间的变化如下表:
①能说明该反应已达到平衡状态的是BCD.
A.v(NO2)正=v(O2)逆 B.容器内压强保持不变
C.v(NO)逆=2v(O2)正D.容器内气体颜色不变
②能使该反应的反应速率增大,且平衡向正反应方向移动的措施是BC.
A.适当升高温度 B.缩小反应容器的体积C.增大O2的浓度 D.选择高效催化剂.
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.①图中E1代表的意义是反应物的活化能.
该反应是放热反应(填“吸热”或“放热”).反应热△H的表达式为E1-E2 .
②当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”).
(2)800℃时,在2L密闭容器内充入0.50mol NO和0.25mol O2,发生如下反应:2NO(g)+O2(g)═2NO2(g)△H<0.体系中,n(NO)随时间的变化如下表:
| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.50 | 0.35 | 0.28 | 0.25 | 0.25 | 0.25 |
A.v(NO2)正=v(O2)逆 B.容器内压强保持不变
C.v(NO)逆=2v(O2)正D.容器内气体颜色不变
②能使该反应的反应速率增大,且平衡向正反应方向移动的措施是BC.
A.适当升高温度 B.缩小反应容器的体积C.增大O2的浓度 D.选择高效催化剂.
5.下列有关实验装置进行的相应实验,能达到实验目的是( )
| A. |  蒸发FeCl3溶液得氯化铁晶体 蒸发FeCl3溶液得氯化铁晶体 | |
| B. |  测量氯气的体积 测量氯气的体积 | |
| C. |  作为制取少量SO2的尾气吸收装置 作为制取少量SO2的尾气吸收装置 | |
| D. |  制备Fe(OH)2并能较长时间观察其颜色 制备Fe(OH)2并能较长时间观察其颜色 |