题目内容
11.图中各装置,能组成原电池的是( )| A. |  | B. |  | C. |  | D. |  |
分析 原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,以此解答该题.
解答 解:A.乙醇不导电,不能形成原电池,故A错误;
B.两电极材料不同,锌较活泼能和稀硫酸自发的进行氧化还原反应,且构成了闭合回路,所以能构成原电池,故B正确;
C.电极相同不能形成电势差,不能形成原电池,故C错误;
D.没有形成闭合回路,不能形成原电池,故D错误.
故选B.
点评 本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,明确原电池的构成条件是解本题关键,根据原电池的构成条件来分析解答即可,题目难度不大.

练习册系列答案
相关题目
1.下列各组离子一定能大量共存的是( )
| A. | 在强碱溶液中:Na+.K+.AlO2-.CO32- | |
| B. | 在含大量Fe3+的溶液中:NH4+.Na+.Cl-.SCN- | |
| C. | 在c(H+)=10-13mol/L 的溶液中:NH4+.Al3+.SO42-.NO3- | |
| D. | 在pH=1的溶液中:K+.Fe2+.Cl-.NO3- |
19.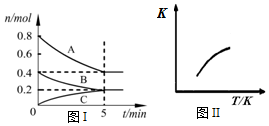 固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )
固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )
 固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )
固定容积为2L的密闭容器中发生反应xA(g)+yB(g)?zC(g),图I表示200℃时容器中各物质的量随时间的变化关系,图II表示平衡时平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( )| A. | 200℃时,反应从开始到平衡的平均速率v(A)=0.08 mol•L-1•min-1 | |
| B. | 200℃时,若在第6 min再向体系中充入1 mol He,此时v(正)>v(逆) | |
| C. | 若0~5 min内容器与外界的热交换总量为m kJ,则该反应的热化学方程式可表示为:2A(g)+B(g)?C(g)△H=+5m kJ/mol | |
| D. | 200℃时,平衡后再充入2 mol C,则再次达到平衡时,C的体积分数等于0.25 |
6.某有机物的结构简式如图所示,下列命名正确的是( )


| A. | 2,3,3-三甲基戊烷 | B. | 3,3,4-三甲基己烷 | ||
| C. | 2,3-二甲基-3-乙基丁烷 | D. | 2-乙基-2,3-二甲基丁烷 |
16.五种短周期主族元素A、B、C、D、E的原子序数依次增大,A2属于绿色燃料,C的氧化物用于生产光导纤维,D元素原子的核电荷数是同主族上一周期元素的2倍,B、C为同周期元素,B、D原子最外层电子数之和等于E的最外层电子数. 根据以上叙述,下列说法中正确的是( )
| A. | 五种元素中有两种金属元素 | |
| B. | 元素C、D、E的最高价氧化物对应水化物的酸性增强 | |
| C. | 元素D、E分别与元素A形成化合物的稳定性:A2D>AE | |
| D. | 元素B、D、E的简单离子半径大小为:B>D>E |
3.下列橡胶产品中属特种橡胶的是( )
| A. | 丁苯橡胶 | B. | 顺丁橡胶 | C. | 氯丁橡胶 | D. | 聚硫橡胶 |
1.同在室温下,同种规格的铝片分别与下列物质混合,反应速率最大的是( )
| A. | 0.1mol/L的HCl 95mL | B. | 0.2mol/L的HCl 90mL | ||
| C. | 0.15mol/L的H2SO410mL | D. | 18mol/L的H2SO485mL |