题目内容
3.分类是化学学习与研究的常用方法,下列分类正确的是( )| A. | Cl2O7、P2O5、SO3、CO2、NO2均属于酸性氧化物 | |
| B. | K2O、K2O2、KO2为相同元素组成的金属氧化物,都属于碱性氧化物 | |
| C. | 根据能否发生丁达尔效应,可以区分胶体和溶液 | |
| D. | 根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
分析 酸性氧化物是能和碱反应生成盐和水的氧化物;碱性氧化物是能和酸反应生成盐和水的氧化物;三大分散系中只有胶体会发生丁达尔效应;根据溶液是否完全电离,将电解质分为强电解质、弱电解质.
解答 解:A、Cl2O7、P2O5、SO3、CO2属于酸性氧化物,NO2不属于酸性氧化物,故A错误;
B、K2O2和酸反应生成盐、水和氧气,不属于碱性氧化物,故B错误;
C、三大分散系中只有胶体会发生丁达尔效应,根据能否发生丁达尔效应,可以区分胶体和溶液,故C正确;
D、根据溶液是否完全电离,将电解质分为强电解质、弱电解质,故D错误.
故选C.
点评 本题考查了酸性氧化物、碱性氧化物、强电解质、弱电解质等基本概念知识,难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
13.由实验事实得出的结论,其中正确的是( )
| 实验事实 | 结论 | |
| A | Cl2的水溶液能导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | 金属钠与乙醇反应不如钠与水反应剧烈 | 乙醇分子中的羟基氢原子不如水分子中的氢原子活泼 |
| D | 加热煮沸滴有石蕊试液的SO2水溶液,红色褪去 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
11.下列物质由离子构成的是( )
| A. | 铜 | B. | 二氧化碳 | C. | 金刚石 | D. | 氯化钠 |
18.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 7.1g C12与足量NaOH溶液反应转移的电子数为0.2NA | |
| B. | 46 g NO2 和 N2O4混合气体中含有原子数为3NA | |
| C. | 1mol Na2O2 固体中含离子总数为4NA | |
| D. | 标准状况下,2.24L辛烷所含分子数为0.1NA |
15.在密闭容器中发生反应:X2(g)+3Y2(g)?2Z(g),其中X2、Y2、Z的起始浓度依次为0.3mol•L-1、0.3mol•L-1、0.2mol•L-1,当反应达到平衡时,各物质的浓度有可能的是( )
| A. | c(X2)=0.1mol•L-1 | B. | c(Y2)=0.3mol•L-1 | C. | c(X2)=0.2mol•L-1 | D. | c(Z)=0.3mol•L-1 |
12.能正确表示下列反应的离子方程式的是( )
| A. | 向FeI2溶液中加入少量氯水2Fe2++Cl2=2Fe3++2Cl- | |
| B. | NaClO (aq) 中通入过量 SO2:C1O-+SO2+H2O=HClO+HSO3- | |
| C. | 氯气通入水中:Cl2+H2O=2H++Cl-+ClO- | |
| D. | 次氯酸钙溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2 HClO |
11.某化学研究性学习小组拟利用下列装置和药品进行四氯化锡的制备.供选择的药品:4.8gSn、浓HCl、稀HCl、浓H2SO4、MnO2、KMnO4、无水CaCl2、碱石灰.
仪器装置:
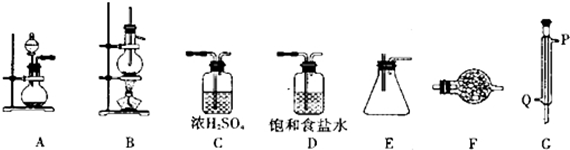
已知四氯化锡具有强的吸水性,水解生成锡的氧化物.SnCl4和Sn的部分数据如下:
请回答下列相关问题:
(1)实验时装置的正确连接顺序为A→D→C→B→G→E→F
(2)仪器G的名称是冷凝管实验时,冷却水的流向是从Q进入(填符号)
(3)A中反应的离子方程式2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(4)F中盛装的化学试剂是碱石灰;作用是防止空气中的水分进入装置E中、吸收多余的Cl2防止污染.写出SnCl4水解的化学方程式SnCl4+4H2O=Sn(OH)4+4HCl.
(5)实验完毕后,E装置质量增加9.4g,SnCl4的产率是90%.
仪器装置:

已知四氯化锡具有强的吸水性,水解生成锡的氧化物.SnCl4和Sn的部分数据如下:
| 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | |
| 四氯化锡 | 2.2 | -33 | 114 |
| 金属锡 | 5.77 | 231 |
(1)实验时装置的正确连接顺序为A→D→C→B→G→E→F
(2)仪器G的名称是冷凝管实验时,冷却水的流向是从Q进入(填符号)
(3)A中反应的离子方程式2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(4)F中盛装的化学试剂是碱石灰;作用是防止空气中的水分进入装置E中、吸收多余的Cl2防止污染.写出SnCl4水解的化学方程式SnCl4+4H2O=Sn(OH)4+4HCl.
(5)实验完毕后,E装置质量增加9.4g,SnCl4的产率是90%.