题目内容
下列离子方程式书写正确的是( )
| A、0.1mol/LNH4CN溶液呈碱性,是因溶液中只存在:CN-+H2O?HCN+OH- | ||
| B、CuSO4溶液中加入过量氨水反应:Cu2++4NH3?H2O=[Cu(NH3)4]2++H2O | ||
| C、Fe(OH)3与强酸氢碘酸反应:Fe(OH)3+3H+=Fe3++3H2O | ||
D、甲醛与足量银氨溶液反应:HCHO+2[Ag(NH3)2]++2OH-
|
考点:离子方程式的书写
专题:
分析:A.氨根离子为弱碱阳离子,氰酸根离子为弱酸根离子,二者都水解,溶液呈碱性是因为氰酸根离子水解能力强于氨根离子;
B.CuSO4溶液中加入过量氨水反应,先反应生成氢氧化铜沉淀,然后再发生络合反应生成可溶性络合物;
C.三价铁离子能够氧化碘离子;
D.1mol甲醛与4mol银氨溶液反应.
B.CuSO4溶液中加入过量氨水反应,先反应生成氢氧化铜沉淀,然后再发生络合反应生成可溶性络合物;
C.三价铁离子能够氧化碘离子;
D.1mol甲醛与4mol银氨溶液反应.
解答:
解:A.0.1mol/LNH4CN溶液,存在氨根离子的水解:NH4++H2O NH3?H2O+H+,存在CN-的水解:CN-+H2O?HCN+OH-,溶液呈碱性是因为氰酸根离子水解能力强于氨根离子,故A错误;
B.CuSO4溶液中加入过量氨水反应,离子方程式为:Cu2++4NH3?H2O=[Cu(NH3)4]2++H2O,故B正确;
C.Fe(OH)3与强酸氢碘酸反应,离子方程式:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,故C错误;
D.甲醛与足量银氨溶液反应:HCHO+4[Ag(NH3)2]++4OH-
4Ag↓+CO32-+2NH4++6NH3↑+2H2O,故D错误;
故选:B.
B.CuSO4溶液中加入过量氨水反应,离子方程式为:Cu2++4NH3?H2O=[Cu(NH3)4]2++H2O,故B正确;
C.Fe(OH)3与强酸氢碘酸反应,离子方程式:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,故C错误;
D.甲醛与足量银氨溶液反应:HCHO+4[Ag(NH3)2]++4OH-
| △ |
故选:B.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意反应物用量对反应的影响,选项BD为易错选项.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列事实不能用勒夏特列原理解释的是( )
| A、高压有利于氨的合成 |
| B、加热含有酚酞的纯碱溶液,溶液红色变深 |
| C、向AgCl悬浊液中加入NaI溶液有AgI生成 |
| D、使用催化剂可加快SO2转化为SO3的反应速率 |
已知R为短周期元素,该元素原子的最外层电子数比次外层电子数少3个,则该元素最高价氧化物的分子式为( )
| A、R2O3 |
| B、R2O5 |
| C、RO2 |
| D、RO3 |
设阿伏伽德罗常数为NA,则下列说法正确的是( )
| A、15g甲基所含有的电子数是10NA |
| B、碳原子数为n的饱和一元醇1mol所含共价键数为(3n+3)NA |
| C、标准状况下,22.4L乙烷充分燃烧后生成的气态产物的分子数为6NA |
| D、2.8g己烯和聚丙烯的混合物中所含碳原子数为0.2NA |
下列反应的方程式书写正确的( )
A、氯乙烷消去反应制乙烯:CH3CH2Cl
| |||
B、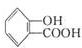 +2Na2CO3→ +2Na2CO3→ +2NaHCO3 +2NaHCO3 | |||
| C、苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |||
D、甲醛溶液中加入足量的银氨溶液并水浴加热:HCHO+2[Ag(NH3)2]+2OH-
|
下列有机物命名正确的是( )
A、1,3,4-三甲苯  |
B、2-甲基-2-氯丙烷 |
C、2-甲基-1-丙醇 |
D、2-甲基-3-丁炔 |
 乙醇的分子组成为C2H6O,现采用实验方法确定一个乙醇分子里有几个氢原子能被钠置换.测试装置如图所示.
乙醇的分子组成为C2H6O,现采用实验方法确定一个乙醇分子里有几个氢原子能被钠置换.测试装置如图所示.
