题目内容
已知反应:A(g)+2B(g)?3C(g)在一定温度下达到平衡.
(1)该反应的平衡常数表达式为 .
(2)若各物质的平衡浓度分别为c(A)=2.0mol/L、c(B)=2.0mol/L、c(C)=1.0mol/L,则K= .
(3)一定温度下,能说明反应已达到平衡的是 .
①C生成速率与C分解速率相等 ②单位时间内消耗a mol A,同时生成3a mol C
③容器内的压强不再变化 ④混合气体的物质的量不再变化
(4)保持温度不变,将容器的容积扩大到原来的两倍,下列有关判断正确的是 .
①平衡向正反应方向移动 ②B的转化率不变 ③C的体积分数增大.
(1)该反应的平衡常数表达式为
(2)若各物质的平衡浓度分别为c(A)=2.0mol/L、c(B)=2.0mol/L、c(C)=1.0mol/L,则K=
(3)一定温度下,能说明反应已达到平衡的是
①C生成速率与C分解速率相等 ②单位时间内消耗a mol A,同时生成3a mol C
③容器内的压强不再变化 ④混合气体的物质的量不再变化
(4)保持温度不变,将容器的容积扩大到原来的两倍,下列有关判断正确的是
①平衡向正反应方向移动 ②B的转化率不变 ③C的体积分数增大.
考点:化学平衡常数的含义,化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:(1)依据化学方程式和平衡常数概念书写表达式,用生成物平衡浓度的幂次方乘积除以反应物平衡浓度的幂次方乘积得到;
(2)依据平衡浓度和平衡常数计算式列式计算得到;
(3)化学平衡状态时正逆反应速率相同,各组分含量保持不变,以及衍生出的其他判断依据;
(4)保持温度不变,将容器的容积扩大到原来的两倍,压强减小,反应是前后气体体积不变的反应,平衡不动.
(2)依据平衡浓度和平衡常数计算式列式计算得到;
(3)化学平衡状态时正逆反应速率相同,各组分含量保持不变,以及衍生出的其他判断依据;
(4)保持温度不变,将容器的容积扩大到原来的两倍,压强减小,反应是前后气体体积不变的反应,平衡不动.
解答:
解:(1)A(g)+2B(g)?3C(g)在一定温度下达到平衡,反应的平衡常数K=
;
故答案为:
;
(2)若各物质的平衡浓度分别为c(A)=2.0mol/L、c(B)=2.0mol/L、c(C)=1.0mol/L,则平衡常数K=
=
=0.125;
故答案为:0.125;
(3)A(g)+2B(g)?3C(g)在一定温度下达到平衡,改变条件,依据化学平衡移动原理分析选项;
①C生成速率与C分解速率相等,说明C的正逆反应速率相同,说明反应达到平衡状态,故①符合;
②单位时间内消耗a mol A,同时生成3a mol C,只能说明反应正向进行,不能说明反应达到平衡状态,故②不符合;
③反应前后气体物质的量相同,过程中和平衡状态下压强不变,容器内的压强不再变化,不能说明反应达到平衡状态,故③不符合;
④混反应前后气体物质的量相同,合气体的物质的量不再变化,不能说明反应大大平衡状态,故④不符合;
故答案为:①;
(4)保持温度不变,将容器的容积扩大到原来的两倍,压强减小,反应是前后气体体积不变的反应,平衡不动,反应物转化率不变,C的体积分数不变;
故答案为:②.
| c3(C) |
| c(A)c2(B) |
故答案为:
| c3(C) |
| c(A)c2(B) |
(2)若各物质的平衡浓度分别为c(A)=2.0mol/L、c(B)=2.0mol/L、c(C)=1.0mol/L,则平衡常数K=
| c3(C) |
| c(A)c2(B) |
| 1.03 |
| 2.0×2.02 |
故答案为:0.125;
(3)A(g)+2B(g)?3C(g)在一定温度下达到平衡,改变条件,依据化学平衡移动原理分析选项;
①C生成速率与C分解速率相等,说明C的正逆反应速率相同,说明反应达到平衡状态,故①符合;
②单位时间内消耗a mol A,同时生成3a mol C,只能说明反应正向进行,不能说明反应达到平衡状态,故②不符合;
③反应前后气体物质的量相同,过程中和平衡状态下压强不变,容器内的压强不再变化,不能说明反应达到平衡状态,故③不符合;
④混反应前后气体物质的量相同,合气体的物质的量不再变化,不能说明反应大大平衡状态,故④不符合;
故答案为:①;
(4)保持温度不变,将容器的容积扩大到原来的两倍,压强减小,反应是前后气体体积不变的反应,平衡不动,反应物转化率不变,C的体积分数不变;
故答案为:②.
点评:本题考查了化学平衡影响因素分析,平衡常数的计算,平衡标志是解题关键,掌握平衡移动原理和实质是关键,题目较简单.

练习册系列答案
相关题目
 如图装置中X和Y均为石墨电极,电解液为500mL某蓝色溶液,电解一段时间,观察到X电极表面有红色的固态物质生成,Y电极有无色气体生成;溶液中原有溶质完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极增重1.6g.下列有关说法中不正确的是( )
如图装置中X和Y均为石墨电极,电解液为500mL某蓝色溶液,电解一段时间,观察到X电极表面有红色的固态物质生成,Y电极有无色气体生成;溶液中原有溶质完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极增重1.6g.下列有关说法中不正确的是( )| A、X电极是阴极 |
| B、Y电极产生气体的体积为0.224L |
| C、电解后溶液的pH=1 |
| D、要使电解后溶液恢复到电解前的状态,需加入一定量的CuO或CuCO3 |
如图是印在食品包装内常见小袋子上的部分图案,该小袋子内的物质最有可能是( )


| A、铁粉 | B、氧化钠 |
| C、亚硫酸钠 | D、生石灰 |
下列反应能设计成原电池提供电能的是( )
| A、Cu与Cl2燃烧反应 |
| B、Ba(OH)2?8H2O与NH4Cl反应 |
| C、灼热的炭与CO2反应 |
| D、氢氧化钠溶液与稀盐酸反应 |
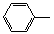 -CH=CH2)和D(HO-
-CH=CH2)和D(HO-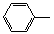 -CHO)按如下方法合成:
-CHO)按如下方法合成: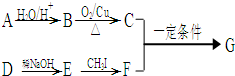
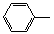 -ONa+RCH2I→
-ONa+RCH2I→ -OCH2R
-OCH2R