题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、39g苯分子中含有的碳碳双键数为1.5NA |
| B、少量CH3COOH和1mol CH3COONa溶于水所得中性溶液中,CH3COO-数目为NA |
| C、2.24L NH3中含共价键数目一定为0.3NA |
| D、5.6g Fe投入100mL 3.5mol?L-1稀硝酸中,充分反应,转移电子总数为0.3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.苯分子中的碳碳键为一种独特键,不存在碳碳双键;
B.根据电荷守恒及溶液为中性的特点判断醋酸根离子的数目;
C.没有告诉标况下,不能使用标况下的气体摩尔体积计算2.24L氨气的物质的量;
D.铁与稀硝酸反应生成铁离子的方程式为:Fe+4H++NO3-═Fe3++NO↑+2H2O,根据铁与稀硝酸的物质的量判断反应产物.
B.根据电荷守恒及溶液为中性的特点判断醋酸根离子的数目;
C.没有告诉标况下,不能使用标况下的气体摩尔体积计算2.24L氨气的物质的量;
D.铁与稀硝酸反应生成铁离子的方程式为:Fe+4H++NO3-═Fe3++NO↑+2H2O,根据铁与稀硝酸的物质的量判断反应产物.
解答:
解:A.苯分子中的碳碳键是一种介于单键和双键之间的独特键,不存在碳碳双键,故A错误;
B.醋酸与醋酸钠的混合液为中性,则氢离子与氢氧根离子浓度相等,根据电荷守恒,钠离子与醋酸根离子的物质的量相等,所以醋酸根离子的物质的量为1mol,CH3COO-数目为NA,故B正确;
C.不是标准状况下,题中条件无法计算2.24L氨气的物质的量及共价键数目,故C错误;
D.5.6g铁的物质的量为0.1mol,100mL 3.5mol?L-1稀硝酸的物质的量为0.35mol,根据反应Fe+4H++NO3-═Fe3++NO↑+2H2O可知,0.1mol铁完全反应生成铁离子,消耗硝酸的物质的量为4mol,显然硝酸不足,反应后有亚铁离子生成,所以转移的电子的物质的量小于0.3mol,故D错误;
故选B.
B.醋酸与醋酸钠的混合液为中性,则氢离子与氢氧根离子浓度相等,根据电荷守恒,钠离子与醋酸根离子的物质的量相等,所以醋酸根离子的物质的量为1mol,CH3COO-数目为NA,故B正确;
C.不是标准状况下,题中条件无法计算2.24L氨气的物质的量及共价键数目,故C错误;
D.5.6g铁的物质的量为0.1mol,100mL 3.5mol?L-1稀硝酸的物质的量为0.35mol,根据反应Fe+4H++NO3-═Fe3++NO↑+2H2O可知,0.1mol铁完全反应生成铁离子,消耗硝酸的物质的量为4mol,显然硝酸不足,反应后有亚铁离子生成,所以转移的电子的物质的量小于0.3mol,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确苯中碳碳键情况及标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为难点和易错点,注意根据反应物的量正确判断反应产物.

练习册系列答案
相关题目
对于反应A(g)+B(s)?2C(g)△H<0 该反应达到平衡后,下列条件有利于平衡向正反应方向移动的是( )
| A、降低温度和减小压强 |
| B、升高温度和增大压强 |
| C、降低温度和增大压强 |
| D、升高温度和减小压强 |
在密闭容器中充入4mol A,在一定温度和体积可变的密闭容器中发生如下反应:4A(g)═3B(g)+C(g)△H<0,达到平衡时有30%的A发生反应,下列判断正确的是( )
| A、若向密闭体系内再加入3mol B、2mol C,达平衡时C的百分含量与原平衡相同 |
| B、达到平衡时气体的总物质的量、密度都不发生变化 |
| C、反应达平衡的过程中,释放出的热量不发生变化 |
| D、升高温度A的转化率大于30% |
X、Y、Z、W、R属于短周期元素.已知它们都不是稀有气体元素,X的原子半径短周期最大,Y元素的原子最外层电子数为m,次层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1. 下列叙述错误的是( )
| A、X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 |
| B、Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物高 |
| C、Z、W、R最高价氧化物对应水化物的酸性强弱顺序是R>W>Z |
| D、Y分别与Z、W、R以两种元素组成的常见化合物有5种,且它们晶体类型相同 |
根据以下叙述制备氯化铜:将含有FeO杂质的CuO粉末慢慢加入浓盐酸中,充分反应后粉末溶解.已知:FeS不溶于水,但溶于强酸.
在除去溶液中的Fe2+时,可采用的方法是( )
| 溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥9.6 | ≥6.4 |
| A、加入纯铜粉,将Fe2+还原为Fe |
| B、直接加NaOH溶液,调整溶液的pH≥9.6 |
| C、先将Fe2+氧化成Fe3+,再调整溶液pH至3.7~4 |
| D、通入H2S使Fe2+直接沉淀 |
在元素周期表中,第二、第三、第四、第五、第六周期元素的种数分别是( )
| A、8、8、18、18、36 |
| B、8、8、18、32、32 |
| C、8、8、18、18、32 |
| D、8、18、18、36、36 |
下列表示反应中电子转移的方向和数目正确的是( )
A、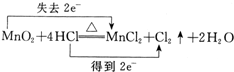 |
B、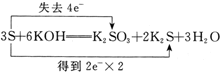 |
C、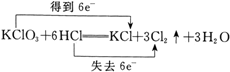 |
D、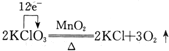 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1mol Na2O和1mol Na2O2中,含阴离子的数目均为NA |
| B、标准状况下,1mol Cl2溶于水,转移电子的数目为NA |
| C、含2mol H2SO4 的浓硫酸与足量铜粉完全反应,生成气体分子的数目为2NA |
| D、将含Na+数目为NA的NaCl固体溶于1L水中,所得溶液的浓度为1mol?L-1 |