题目内容
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1mol Na2O和1mol Na2O2中,含阴离子的数目均为NA |
| B、标准状况下,1mol Cl2溶于水,转移电子的数目为NA |
| C、含2mol H2SO4 的浓硫酸与足量铜粉完全反应,生成气体分子的数目为2NA |
| D、将含Na+数目为NA的NaCl固体溶于1L水中,所得溶液的浓度为1mol?L-1 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.过氧化钠的阴离子为过氧根离子,1mol Na2O和1mol Na2O2中都含有1mol阴离子;
B.氯气溶于水中,只有少量的氯气与水反应生成氯化氢和次氯酸;
C.随着反应的进行,浓硫酸会变成稀硫酸,稀硫酸与铜不反应,所以生成的二氧化碳的物质的量减小;
D.氯化钠溶于1L水中,所得溶液的体积不是1L.
B.氯气溶于水中,只有少量的氯气与水反应生成氯化氢和次氯酸;
C.随着反应的进行,浓硫酸会变成稀硫酸,稀硫酸与铜不反应,所以生成的二氧化碳的物质的量减小;
D.氯化钠溶于1L水中,所得溶液的体积不是1L.
解答:
解:A.1mol Na2O和1mol Na2O2中都含有1mol阴离子,含阴离子的数目均为NA,故A正确;
B.1mol Cl2溶于水,只有部分氯气与水反应生成氯化氢和次氯酸,所以转移的电子的物质的量小于1mol,故B错误;
C.铜与浓硫酸的反应中,反应消耗2mol浓硫酸,会生成1mol二氧化硫,由于随着反应的进行,浓硫酸浓度减小,最后浓硫酸变成稀硫酸后,稀硫酸与铜不反应,所以生成的二氧化硫的物质的量小于1mol,生成气体分子的数目小于NA,故C错误;
D.将含Na+数目为NA的NaCl固体溶于1L水中,所得溶液体积不是1L,浓度不是1mol?L-1,故D错误;
故选A.
B.1mol Cl2溶于水,只有部分氯气与水反应生成氯化氢和次氯酸,所以转移的电子的物质的量小于1mol,故B错误;
C.铜与浓硫酸的反应中,反应消耗2mol浓硫酸,会生成1mol二氧化硫,由于随着反应的进行,浓硫酸浓度减小,最后浓硫酸变成稀硫酸后,稀硫酸与铜不反应,所以生成的二氧化硫的物质的量小于1mol,生成气体分子的数目小于NA,故C错误;
D.将含Na+数目为NA的NaCl固体溶于1L水中,所得溶液体积不是1L,浓度不是1mol?L-1,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项D为易错点,注意所得溶液的体积不是1L.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、39g苯分子中含有的碳碳双键数为1.5NA |
| B、少量CH3COOH和1mol CH3COONa溶于水所得中性溶液中,CH3COO-数目为NA |
| C、2.24L NH3中含共价键数目一定为0.3NA |
| D、5.6g Fe投入100mL 3.5mol?L-1稀硝酸中,充分反应,转移电子总数为0.3NA |
下列有关试剂的保存方法正确的是.( )
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④白磷保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中.
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④白磷保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中.
| A、①③⑤ | B、②③⑤ |
| C、②④⑤ | D、①③④ |
标准状况下,32g某气体的分子数与22gCO2的分子数相同,则该气体的摩尔质量为( )
| A、32 |
| B、32 g/mol |
| C、64g/mol |
| D、64 |
下列操作正确且能达到预期目的是( )
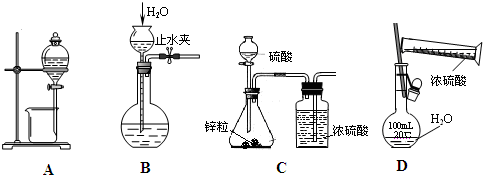

| A、分离酒精和水 |
| B、检查气体发生装置的气密性 |
| C、用Zn粒和稀硫酸制备干燥的H2 |
| D、用浓硫酸配制100mL 1.0mol/L的稀硫酸 |
新能源的特点是资源丰富,无污染或很少污染,且可以再生.下列属于新能源的是( )
| A、太阳能 | B、石油 | C、天然气 | D、煤 |
下列物质中,不能用金属单质跟非金属单质直接化合制得的是( )
| A、FeS |
| B、FeCl2 |
| C、CuCl2 |
| D、CuO |
2006年1月,河南省某电厂柴油泄漏污染黄河水,使山东等省纷纷发布预警,关闭沿河取水口.泄漏的柴油或含油污水进入自然水体后,对水生生物产生很大影响.下列叙述中,错误的是( )
| A、柴油油膜阻止了氧气溶解,使水中氧气得不到补充而缺氧,水质变差 |
| B、油膜粘附在鱼身上,使鱼不能正常生活 |
| C、油污粘附在植物茎叶上,使植物死亡 |
| D、油膜通常很薄,对水生生物的影响极其微小 |