题目内容
下列有关二氧化硅的叙述中不正确的是( )
| A、沙子、石英、水晶的主要成分都是SiO2 |
| B、SiO2是制光导纤维的主要原料 |
| C、硅酸可由SiO2直接制得 |
| D、SiO2是酸性氧化物,一定条件下可与碱性氧化物或碱反应 |
考点:硅和二氧化硅
专题:碳族元素
分析:A.石英、水晶的主要成分都是SiO2;
B.光导纤维的主要成分是二氧化硅;
C.二氧化硅不溶于水,与水不反应;
D.酸性氧化物指与碱反应生成盐与水的氧化物.
B.光导纤维的主要成分是二氧化硅;
C.二氧化硅不溶于水,与水不反应;
D.酸性氧化物指与碱反应生成盐与水的氧化物.
解答:
解:A.沙子、石英、水晶的主要成分都是二氧化硅,故A错误;
B.制造光导纤维的主要材料是SiO2,故B错误;
C.二氧化硅不溶于水,与水不反应,二氧化硅不能一步反应得到硅酸,故C正确;
D.酸性氧化物指与碱反应生成盐与水的氧化物,一定条件下均能与碱性氧化物或碱发生反应,故D错误.
故选C.
B.制造光导纤维的主要材料是SiO2,故B错误;
C.二氧化硅不溶于水,与水不反应,二氧化硅不能一步反应得到硅酸,故C正确;
D.酸性氧化物指与碱反应生成盐与水的氧化物,一定条件下均能与碱性氧化物或碱发生反应,故D错误.
故选C.
点评:本题考查硅及其化合物和酸性氧化物等知识,难度中等,需要学生对元素化合物知识掌握全面.

练习册系列答案
相关题目
下列括号中的分离方法运用得当的是( )
| A、植物油和自来水(蒸馏) |
| B、水溶液中的食盐和碘(分液) |
| C、CaCO3和CaCl2(溶解、过滤、蒸发) |
| D、自来水中的杂质(萃取) |
能正确表示下列反应的离子方程式是( )
| A、Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O | ||||
| B、铝粉与NaOH溶液反应:2Al+2OH-=2AlO2-+H2↑ | ||||
| C、5.6g Fe与200mL 2.0mol/L HNO3溶液充分反应:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O | ||||
D、碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-
|
烧碱溶液与稀盐酸的反应,属于( )
| A、放热反应 |
| B、吸热反应 |
| C、既是放热反应也是吸热反应 |
| D、既不是放热反应也不是吸热反应 |
将来科学家要在月球上进行科学研究,下列实验操作中在月球表面难以完成的是( )
| A、蒸馏 | B、溶解 | C、过滤 | D、蒸发 |
下列有关电解质溶液微粒关系比较一定正确的是( )
| A、氨水和氯化铵的混合液,当pH=7时,c (Cl一)>c (NH4+) |
| B、pH=2的一元酸和pH=12的NaOH溶液等体积混合,混合液中c(H+)一定等于c (OH-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(CH3COO一)>c(Na+)>c(H+)>c(OH-) |
| D、pH=1的H2SO4与0.10mol?L-1Ba(OH)2溶液以等体积混合的溶液中,水电离出的c(H+)=10-13mol/L |
下列各项反应对应的图象正确的是( )
A、 25℃时,向亚硫酸溶液中通入氯气 |
B、 向NaAlO2溶液中通入HCl气体 |
C、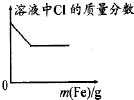 向少量氯化铁溶液中加入铁粉 |
D、 向BaSO4饱和溶液中加入硫酸钠 |
用水热法制备Fe3O4纳米颗粒的总反应如下:3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O.下列说法正确的是( )
| A、在反应中硫元素被氧化,铁元素被还原 |
| B、还原剂是Fe2+,氧化剂是S2O32-和O2 |
| C、当转移1mol电子时,消耗56g S2O32- |
| D、每生成1mol Fe3O4,转移3mol电子 |
下列溶液中的氯离子浓度与50mL 1mol?L-1的AlCl3溶液中氯离子浓度相等的是( )
| A、150mL 1mol?L-1的NaCl |
| B、25mL 2mol?L-1的FeCl3 |
| C、150mL 3mol?L-1的KCl |
| D、75mL 2mol?L-1的CaCl2 |