题目内容
用水热法制备Fe3O4纳米颗粒的总反应如下:3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O.下列说法正确的是( )
| A、在反应中硫元素被氧化,铁元素被还原 |
| B、还原剂是Fe2+,氧化剂是S2O32-和O2 |
| C、当转移1mol电子时,消耗56g S2O32- |
| D、每生成1mol Fe3O4,转移3mol电子 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O中,Fe元素的化合价升高,S元素的化合价升高,只有氧气中O元素的化合价降低,以此来解答.
解答:
解:A.Fe、S元素被氧化,O元素被还原,故A错误;
B.还原剂为Fe2+、S2O32-,氧化剂为O2,故B错误;
C.由反应可知,转移4mol电子消耗2molS2O32-,则转移1mol电子时,消耗0.5molS2O32-,其质量为0.5mol×112g/mol=56g,故C正确;
D.每生成1mol Fe3O4,由电子守恒及O元素的化合价变化可知,转移4mol电子,故D错误;
故选C.
B.还原剂为Fe2+、S2O32-,氧化剂为O2,故B错误;
C.由反应可知,转移4mol电子消耗2molS2O32-,则转移1mol电子时,消耗0.5molS2O32-,其质量为0.5mol×112g/mol=56g,故C正确;
D.每生成1mol Fe3O4,由电子守恒及O元素的化合价变化可知,转移4mol电子,故D错误;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意从化合价角度分析,题目难度中等.

练习册系列答案
相关题目
一定温度下,反应N2+O2?2NO在密闭容器中进行,下列措施不改变化学反应速率的是( )
| A、缩小体积使压强增大 |
| B、恒容,充入N2 |
| C、恒容,充入He |
| D、恒压,充入He |
下列有关二氧化硅的叙述中不正确的是( )
| A、沙子、石英、水晶的主要成分都是SiO2 |
| B、SiO2是制光导纤维的主要原料 |
| C、硅酸可由SiO2直接制得 |
| D、SiO2是酸性氧化物,一定条件下可与碱性氧化物或碱反应 |
2.3g钠投入100g水中,下列叙述述错误的是( )
| A、钠浮在水面,熔化成银色光亮的小球 |
| B、钠贮存在煤油中 |
| C、所得溶液的质量分数为2.25% |
| D、反应中转移0.1mol电子 |
下列说法不正确的是( )
| A、手性异构体性质相同 |
| B、互为手性异构体的分子互为镜像 |
| C、手性异构体分子组成相同 |
| D、手性催化剂只催化或主要催化一种手性分子的合成 |
已知2SO2(g)+O2(g)?2SO3(g) (正反应放热).若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法不正确的是( )
| A、若降低温度,可以减慢反应速率 |
| B、催化剂既能加快化学反应速率,又能提高SO2的转化率 |
| C、氧气足量时,SO2不能完全转化为SO3 |
| D、达到平衡时,SO2和SO3的浓度一定相等 |
关于原子或离子结构的下列说法不正确的是( )
| A、某原子K层上只有一个电子 |
| B、某原子M层上电子数为L层上电子数的4倍 |
| C、某离子M层上和L层上的电子数均为K层的4倍 |
| D、某离子核电荷数与最外层电子数相等 |
下列说法不正确的是( )
| A、体系有序性越高,熵值就越低 |
| B、自发过程将导致体系的熵增大 |
| C、吸热反应不可以自发进行 |
| D、同种物质气态时熵值最大 |
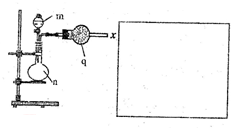 该小组的乙同学利用图所示装置制备并收集干燥的NO2气体.
该小组的乙同学利用图所示装置制备并收集干燥的NO2气体.