题目内容
下列关于微观粒子的说法,正确的是( )
| A、原子是由分子构成的 |
| B、原子中含有质子、中子和核外电子 |
| C、原子若失去核外电子,则会变成阴离子 |
| D、原子若得到核外电子,则会变成阳离子 |
考点:原子构成
专题:原子组成与结构专题
分析:分子是由原子构成的,原子是由原子核和核外电子构成,原子核是由质子和中子构成;若原子失去电子会变成阳离子,得到电子会变成阴离子.
解答:
解:A、原子能构成分子,即分子是由原子构成的;故A错误;
B、原子是由原子核和核外电子构成,原子核是由质子和中子构成;故B正确;
C、若原子失去电子会变成阳离子,故C错误;
D、若原子得到电子会变成阴离子,故D错误;
故选B.
B、原子是由原子核和核外电子构成,原子核是由质子和中子构成;故B正确;
C、若原子失去电子会变成阳离子,故C错误;
D、若原子得到电子会变成阴离子,故D错误;
故选B.
点评:本题考查了分子与原子的联系及原子的构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的.明确原子得失电子会变成阴阳离子.

练习册系列答案
相关题目
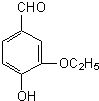 乙基香草醛是食品添加剂的增香原料,其结构简式如图所示,下列对该物质叙述正确的是( )
乙基香草醛是食品添加剂的增香原料,其结构简式如图所示,下列对该物质叙述正确的是( )| A、该物质可以进行消去反应 |
| B、该物质可以进行水解反应 |
| C、1mol该物质最多可与3 mol H2反应 |
| D、该物质可以和溴水发生取代反应 |
下列各醇中,能发生消去反应生成 的是( )
的是( )
 的是( )
的是( )A、 |
| B、CH3-CH2-CH2-CH2OH |
C、 |
D、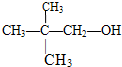 |
21世纪被认为是“海洋世纪”是人类大步走向海洋,开发利用海洋的世纪.下列有关海水资源的开发利用说法正确的是( )
| A、在研究和开发海洋资源时,不能以牺牲环境为代价 |
| B、海水中含有溴元素,可以直接萃取得到溴单质 |
| C、海水中的铀含量极低,从海水中提铀是十分不经济的行为 |
| D、在研究和开发海洋资源时,必要时可以以牺牲环境为代价 |
设NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温下,1L0.1mol/L的NH4NO3溶液中含氮原子数为0.2NA |
| B、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| C、22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D、含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L |
除去下列物质中少量杂质所需除杂试剂及方法不正确的是( )
| 物质(杂质) | 除杂试剂 | 除杂方法 | |
| A | 乙醇(水) | CaO | 蒸馏 |
| B | 淀粉溶液(NaCl) | --- | 渗析 |
| C | CO2(HCl) | NaOH溶液 | 洗气 |
| D | NaCl溶液(I2) | CCl4 | 萃取分液 |
| A、A | B、B | C、C | D、D |
由CH2=CH2→CH3CH2Br→CH3CH2OH→CH3CHO→CH3COOH的转化过程中,经过的反应类型( )
| A、取代→加成→氧化→消去 |
| B、取代→水解→消去→氧化 |
| C、加成→水解→氧化→氧化 |
| D、加成→取代→消去→还原 |
在标准状况下,如果1.6L氧气含n个氧分子,则阿伏加德罗常数的数值为( )
| A、28n | B、14n |
| C、n/28 | D、n/14 |
常温下,0.1mol?L-1某一元酸(HA)溶液中c(OH-)=1×10-11mol?L-1,下列叙述正确的是( )
| A、该一元酸溶液的pH=1 | ||
| B、该溶液中水的离子积常数为1×10-22 | ||
| C、该溶液中HA的电离度为 0.1% | ||
D、若加水稀释,则
|