题目内容
设NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温下,1L0.1mol/L的NH4NO3溶液中含氮原子数为0.2NA |
| B、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| C、22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D、含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol/L |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据氮元素守恒分析判断;
B、乙烯和丁烯最简式相同为CH2,计算21.0gCH2中碳原子数;
C、气体体积温度压强不知,不能计算气体物质的量;
D、含NA个Na+的Na2O溶解于1 L水中,氧化钠和水反应生成氢氧化钠,溶质氢氧化钠物质的量为1mol,溶液体积不是1L.
B、乙烯和丁烯最简式相同为CH2,计算21.0gCH2中碳原子数;
C、气体体积温度压强不知,不能计算气体物质的量;
D、含NA个Na+的Na2O溶解于1 L水中,氧化钠和水反应生成氢氧化钠,溶质氢氧化钠物质的量为1mol,溶液体积不是1L.
解答:
解:A、依据氮元素守恒分析,1L0.1mol/L的NH4NO3溶液中含氮原子数为0.2NA,故A正确;
B、乙烯和丁烯最简式相同为CH2,计算21.0gCH2中碳原子数=
×NA=1.5NA,故B错误;
C、气体体积温度压强不知,不能计算气体物质的量,故C错误;
D、含NA个Na+的Na2O溶解于1 L水中,氧化钠和水反应生成氢氧化钠,溶质氢氧化钠物质的量为1mol,溶液体积不是1L,故D错误;
故选A.
B、乙烯和丁烯最简式相同为CH2,计算21.0gCH2中碳原子数=
| 21g |
| 14g/mol |
C、气体体积温度压强不知,不能计算气体物质的量,故C错误;
D、含NA个Na+的Na2O溶解于1 L水中,氧化钠和水反应生成氢氧化钠,溶质氢氧化钠物质的量为1mol,溶液体积不是1L,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用分析,微粒结构理解应用,物质的量浓度计算方法,掌握基础是关键,题目较简单.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
现有两种高聚物A、B,已知A能溶于氯仿等有机溶剂,并加热到一定条件下熔融成粘稠的液体,B不溶于任何溶剂,加热不会变软或熔融,则下列叙述中一定不正确的是( )
| A、高聚物A可能具有弹性,B可能没有弹性 |
| B、高聚物A可能是线型高分子材料 |
| C、高聚物A一定是体型高分子材料 |
| D、高聚物B可能是体型高分子材料 |
短周期元素X、Y、Z在元素周期表中的位置如图所示.下列说法正确的是( )
| X | ||
| Y | Z |
| A、原子半径的大小为:Z>Y>X |
| B、若X的一种单质为原子晶体,则含Y元素的盐溶液一定呈酸性 |
| C、若Y可作半导体材料,则X、Z的单质均为分子晶体 |
| D、若Y与Z的核电荷数之和为X的4倍,则X、Z各自形成的氢化物熔沸点:X<Z |
下列除去杂质的方法错误的是( )
| A、用蒸馏的方法分离溴和CCl4的混合物 |
| B、除去Cl2中的少量HCl:通入NaOH溶液,收集气体 |
| C、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| D、除去镁中的铝:加足量的NaOH溶液,过滤 |
下列说法正确的是( )
| A、(CH3)3CCH2C(CH3)=CH2的名称为:2,2,4-三甲基-4-戊烯 |
| B、碳原子数小于或等于8的单烯烃,与HBr加成反应的产物只有一种结构,符合条件的单烯烃有6种 |
C、有机物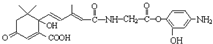 与NaOH溶液反应,最多消耗5mol NaOH 与NaOH溶液反应,最多消耗5mol NaOH |
D、1mol β-紫罗兰酮 ( )与1mol H2发生加成反应可得到3种不同产物 )与1mol H2发生加成反应可得到3种不同产物 |
下列关于微观粒子的说法,正确的是( )
| A、原子是由分子构成的 |
| B、原子中含有质子、中子和核外电子 |
| C、原子若失去核外电子,则会变成阴离子 |
| D、原子若得到核外电子,则会变成阳离子 |
Fe3+和Cu2+能够在滤纸上彼此分离开的原因是( )
| A、饱和氯化铁和硫酸铜已经分层 |
| B、阳光照射使Fe3+和Cu2+能彼此分开 |
| C、滤纸对Fe3+和Cu2+的吸附力不同 |
| D、Fe3+和Cu2+在流动相溶剂中的溶解能力,扩散速度不同 |
要除去下列物质中所混有的杂质(括号内为杂质),所用试剂正确的是( )
| A、KCl(CuCl2)--加过量KOH溶液 |
| B、CO2(SO2)--通过足量NaOH溶液 |
| C、MnO2(KClO3)--加足量的水 |
| D、Na2CO3(Na2SO4)--加足量的BaCl2 |
关于原电池的叙述正确的是( )
| A、构成原电池的正极和负极必须是两种不同金属 |
| B、在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l)△H<0,设计成原电池 |
| C、在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1 120 mL(标准状况)气体析出 |
| D、原电池工作时,正极和负极上发生的都是氧化还原反应 |