题目内容
5.实验测得,某有机物相对分子质量为72.(1)若该有机物是烃,其分子式为C5H12,它有3 种同分异构体.若该烃与Cl2发生取代反应,生成的一氯代物只有1种,则该烃的结构简式为C(CH3)4.
(2)若该有机物3.6g完全燃烧生成0.15molCO2和0.1molH2O,则该有机物的分子式为C3H4O2.若它是一种不饱和羧酸,该酸与甲醇发生酯化反应的化学方程式为(注明反应条件):CH2=CHCOOH+CH3OH$→_{△}^{浓硫酸}$CH2=CHCOOCH3+H2O.
分析 (1)若该有机物是烃,则$\frac{72}{14}$=5…2,故分子式为C5H12;
(2)3.6g有机物中O元素质量为3.6g-0.15mol×12g/mol-0.1mol×2×1g/mol=1.6g,则氧原子物质的量为$\frac{1.6g}{16g/mol}$=0.1mol,故分子中C、H、O原子数目之比为0.15:0.2:0.1=3:4:2,最简式为C3H4O2,相对分子质量为72,故分子式为C3H4O2,若它是一种不饱和羧酸,则其结构简式为CH2=CHCOOH.
解答 解:(1)若该有机物是烃,则$\frac{72}{14}$=5…2,故分子式为C5H12,同分异构体有正戊烷、异戊烷、新戊烷3种,若该烃与Cl2发生取代反应,生成的一氯代物只有1种,则该烃的结构简式为C(CH3)4,
故答案为:C5H12;3;C(CH3)4;
(2)3.6g有机物中O元素质量为3.6g-0.15mol×12g/mol-0.1mol×2×1g/mol=1.6g,则氧原子物质的量为$\frac{1.6g}{16g/mol}$=0.1mol,故分子中C、H、O原子数目之比为0.15:0.2:0.1=3:4:2,最简式为C3H4O2,相对分子质量为72,故分子式为C3H4O2,若它是一种不饱和羧酸,则其结构简式为CH2=CHCOOH,与甲醇发生酯化反应的化学方程式为:CH2=CHCOOH+CH3OH$→_{△}^{浓硫酸}$CH2=CHCOOCH3+H2O,
故答案为:C3H4O2;CH2=CHCOOH+CH3OH$→_{△}^{浓硫酸}$CH2=CHCOOCH3+H2O.
点评 本题考查有机物分子式与结构式确定,掌握根据相对分子质量利用商余法确定烃的分子式,有利于基础知识的巩固.

| A. | CH3C(CH3)2CH3 | B. | CH3CCl3 | C. | CH3CH2OH | D. | CH3CHO |
| A. | 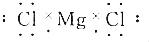 | B. | 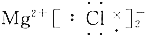 | ||
| C. | 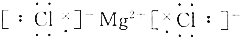 | D. | 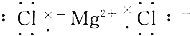 |
| A. | 第七周期ⅣA族 | B. | 第七周期ⅡA族 | C. | 第七周期ⅡB族 | D. | 第六周期ⅥA族 |
| A. | C2H6 | B. | CH3COOH | C. | CH3CH2OH | D. | CH2OHCH2OH |
| A. | Cl | B. | F | C. | S | D. | C |
| A. | H2 D2 | B. | 14N 14C | C. | 16O 17O | D. | O2O3 |
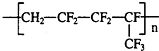 ,合成它的单体为( )
,合成它的单体为( )| A. | CH2=CF2-CF2和CF=CF3 | B. | CH2=CF2和CF2=CF-CF3 | ||
| C. | CH2=CF2=CF2=CF-CF3 | D. | CH2=CF2-CF2=CF-CF3 |
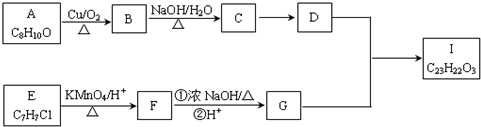
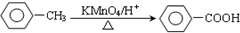
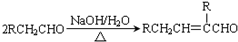
 .
. .
. .
.