题目内容
11.由W、X、Y、Z四种金属按下列装置进行实验.下列说法不正确的是( )| 装置 | 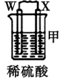 |  | 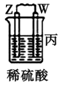 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A. | 装置甲中X电极附近有气泡产生 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH增大 | |
| D. | 四种金属的活动性强弱顺序为W>X>Y>Z |
分析 A.负极失电子逐渐溶解;
B.Y上铜离子得电子生成Cu;
C.W上氢离子得电子生成氢气,溶液中氢离子浓度减小;
D.负极的活泼性大于正极.
解答 解:A.装置甲中金属W不断溶解,负极失电子逐渐溶解,则W作原电池负极,X为正极氢离子得到电子生成氢气,X电极附近有气泡产生,故A正确;
B.Y上铜离子得电子生成Cu,则Y电极上的反应式为Cu2++2e-=Cu,故B正确;
C.W上氢离子得电子生成氢气,溶液中氢离子浓度减小,所以溶液的pH增大,故C正确;
D.甲中W为负极,X为正极,则活动性:W>X;乙中X为负极,Y为正极,则活动性:X>Y;丙中Z为负极,W为正极,则活动性:Z>W,所以四种金属的活动性强弱顺序为Z>W>X>Y,故D错误;
故选D.
点评 本题考查原电池知识,题目难度不大,注意把握原电池中正负极的判断方法以及电极方程式的书写方法,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
7.下列说法中正确的是( )
| A. | 1 mol S和O2的摩尔质量都是32 g | |
| B. | 7.8g Na2S与Na2O2的混合物约含有阴离子6.02×1022个 | |
| C. | 1mol任何气体中都含有相同的原子数 | |
| D. | 22.4LCO2气体中含有3NA个原子 |
2.下列反应中,属于吸热反应的是( )
| A. | 氢氧化钡与氯化铵晶体的反应 | B. | 氢氧化钠与盐酸的反应 | ||
| C. | 锌粒与稀硫酸的反应 | D. | 甲烷在氧气中燃烧 |
6.阿伏伽德罗常数为NA,则下列说法正确的是( )
| A. | 7.8克Na2O2加入100克水中所得溶液中含氧原子0.2NA个 | |
| B. | 标准状况下,11.2LCCl4中含2NA个σ键 | |
| C. | 用惰性电极电解氯化铜溶液,当阳极产生标准状况下黄绿色气体6.72L时,则电路中转移的电子数为0.6NA | |
| D. | 将20.00mL1.5mol/LFeCl3溶液制成胶体,则所得胶体中含有0.03NA个胶粒 |
16.在下列变化中需加入还原剂才能实现的是( )
| A. | KClO3→HCl | B. | Na2O2→O2 | C. | Fe Cl3→FeCl2 | D. | SO2→SO3 |
3.下列有关说法不正确的是( )
| A. | 某有机物化学式为C3H6O2,其核磁共振氢谱有三个峰,其峰的面积比为3:2:1,则该有机物的结构简式一定是CH3CH2COOH | |
| B. | 除去乙酸乙酯中的乙酸和乙醇杂质,可加入足量的饱和纯碱溶液,通过分液即得乙酸乙酯 | |
| C. | 除去乙醇中的少量水,加入新制生石灰,经蒸馏即得乙醇 | |
| D. | 有机物 的系统名称为3-甲基-1-戊烯 的系统名称为3-甲基-1-戊烯 |
9.25℃时,0.1mol/L CH3COOH溶液的pH( )
| A. | =1 | B. | >1 | C. | <1 | D. | =0 |
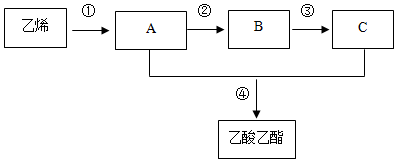
 、
、 ,它们是一种重要的有机合成中间体,D、F为高分子化合物.
,它们是一种重要的有机合成中间体,D、F为高分子化合物.
 +2Cu(OH)2$→_{.}^{△}$
+2Cu(OH)2$→_{.}^{△}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O. $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +2nH2O;
+2nH2O; $→_{.}^{引发剂}$
$→_{.}^{引发剂}$ .
. 是一种医药中间体.请设计合理方案用
是一种医药中间体.请设计合理方案用 合成
合成 (其他原料自选,用反应流程图表示,并注明必要的反应条件).例如:
(其他原料自选,用反应流程图表示,并注明必要的反应条件).例如:
 $→_{光照}^{Cl_{2}}$
$→_{光照}^{Cl_{2}}$ $→_{醇,△}^{NaOH}$
$→_{醇,△}^{NaOH}$ $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$ $→_{浓H_{2}SO_{4},△}^{CH_{3}OH}$
$→_{浓H_{2}SO_{4},△}^{CH_{3}OH}$ .
.