题目内容
9.25℃时,0.1mol/L CH3COOH溶液的pH( )| A. | =1 | B. | >1 | C. | <1 | D. | =0 |
分析 CH3COOH为弱电解质,在溶液中只能部分电离出氢离子,则0.1mol/L CH3COOH溶液中氢离子浓度小于0.1mol/L,据此结合pH=-lgc(H+)分析.
解答 解:醋酸为弱酸,则25℃时0.1mol/L CH3COOH溶液中c(H+)<0.1mol/L,则该溶液的pH>-lg0.1=1,
故选B.
点评 本题考查溶液pH的计算、弱电解质的电离,题目难度不大,明确弱电解质的电离特点为解答关键,注意掌握溶液pH的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.由W、X、Y、Z四种金属按下列装置进行实验.下列说法不正确的是( )
| 装置 | 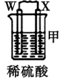 |  | 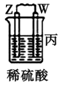 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A. | 装置甲中X电极附近有气泡产生 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH增大 | |
| D. | 四种金属的活动性强弱顺序为W>X>Y>Z |
20.在一恒定的容器中充入3molA和1molB发生反应:3A(g)+B(g)?xC(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.9mol、B:0.3mol、C:2.1mol充入容器,达到平衡后,C的体积分数仍为W%,则x值为( )
| A. | 只能为4 | B. | 只能为3 | ||
| C. | 可能是4,也可能是3 | D. | 无法确定 |
17.下列与有机物的结构、性质有关的叙述正确的是( )
| A. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| B. | 煤的干馏和石油的分馏均属化学变化 | |
| C. | 乙醇可以被氧化为乙酸,二者都能发生取代反应 | |
| D. | 淀粉和蛋白质均可作为生产葡萄糖的原料 |
4.一定量的Fe与过量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入少量( )
| A. | SO3固体 | B. | Zn粉 | C. | K2SO4固体 | D. | CuSO4晶体 |
14.用NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 78g Na2O2中含有的离子总数为4NA | |
| B. | 标准状况下,1.12L HF中所含的分子总数为0.05NA | |
| C. | 由CO2和O2组成的混合物共有NA个分子,其中的氧原子数为2NA | |
| D. | 0.11mol•L-1 FeCl3溶液中含有的Cl-数目为0.3NA |
1.下列物质既能使酸性高锰酸钾溶液又能使溴水(发生化学反应)褪色的是( )
| A. | 乙烯 | B. | 乙烷 | C. | 乙醇 | D. | 苯 |
18. 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )| A. | 该物质与苯酚互为同系物,遇FeCl3溶液呈紫色 | |
| B. | 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4mol和7mol | |
| C. | 该分子中的所有碳原子不可能共平面 | |
| D. | 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键 |
12.对人体健康不会造成危害的事实是( )
| A. | 用工业酒精(含甲醇)兑制饮用白酒 | |
| B. | 用福尔马林浸泡海产品进行防腐保鲜 | |
| C. | 长期饮用长时间反复加热沸腾的水 | |
| D. | 在食用盐中加入碘酸钾以消除碘缺乏病 |