题目内容
10.高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”.这种材料可以按下列方法制备:SiO2$→_{高温}^{①C}$Si(粗)$→_{300℃}^{②HCl}$SiHCl3$→_{1000-1100℃}^{③过量H_{2}}$Si(纯)下列说法正确的是( )
| A. | 步骤①的化学方程式为SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| B. | 步骤①②③中每生成或反应1 mol Si,转移4 mol 电子 | |
| C. | 二氧化硅能与氢氟酸反应,也能与氢氧化钠溶液反应,属于两性氧化物 | |
| D. | SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3 |
分析 A、二氧化硅高温下与C反应生成CO气体;
B、氧化还原反应得失电子守恒判断即可;
C、二氧化硅既能与氢氟酸反应,又能与烧碱反应,但它是酸性氧化物;
D、由沸点可知,为相差30℃以上的两种液体.
解答 解:A、二氧化硅高温下与C反应生成CO气体,即步骤①的化学方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故A错误;
B、步骤①中Si的化合价降低4,转移电子数为4mol,步骤②中生成SiHCl3,化合价升高2,步骤③中每生成1mol Si,转移2mol电子,故B错误;
C、二氧化硅既能与氢氟酸反应,又能与烧碱反应,但二氧化硅和HF反应生成四氟化硅而不是盐,所以它是酸性氧化物而不是两性氧化物,故C错误;
D、沸点相差30℃以上的两种液体可以采用蒸馏的方法分离,故D正确,
故选D.
点评 本题是一道有关硅的无机推断题,考查的知识点范围较广,涉及氧化还原反应原理应用、蒸馏等,可以根据已有知识进行.

练习册系列答案
相关题目
1.“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”在食盐中用NaCl中按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2).
(1)测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
(1)测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%.该样品a的水溶液中,含量最多的离子是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种).请设计实验方案,完成下列表格.
| 实验操作 | 预期现象及结论 |
| 步骤1:取少量样品b于烧杯中,加足量蒸馏水,并用玻璃棒搅拌 | 样品溶解,形成无色溶液. |
| 步骤2:取少量步骤1形成的溶液于试管中,再滴加少量NaOH溶液,振荡 | 有白色沉淀生成,说明样品b中添加了镁盐 |
| 步骤3:取少量步骤1形成的溶液于试管中,再滴加少量的BaCl2溶液振荡 | 若有白色沉淀产生,则添加的是MgSO4.若无明显现象,则添加的是MgCl2 |
5.下列物质中,不属于电解质的是( )
| A. | NaCl | B. | 盐酸 | C. | H2SO4 | D. | KOH |
15.在除杂过程中要尽量除去杂质,加入的试剂必须稍过量,且最后过量物质可以使用物理方法或化学方法除去.现要除去NaCl中少量的CaCl2、Na2SO4杂质,下列选用试剂及使用顺序正确的是( )
| A. | Na2CO3、BaCl2、HCl | B. | BaCl2、Na2CO3、H2SO4 | ||
| C. | BaCl2、Na2CO3、HCl | D. | Ba(NO3)2、Na2CO3、HCl |
2.下列是一些物质粒子的示意图:其中可能属于氧化物的是( )
| A. | 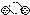 | B. | 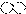 | C. |  | D. |  |
19.已知X、Y、Z、W为原子序数依次增大的短周期主族元素,Z+与X3一具有相同的电子层结构,Y、W原子的价电子数目之和为13.下列有关说法中正确的是( )
| A. | 四种元素的原子半径:Z<Y<X<W | |
| B. | 化合物Z3X与ZX3中的化学键类型相同 | |
| C. | X与W两种元素的最简单氢化物间能发生化合反应 | |
| D. | 常温下,X和Y形成的所有单质均为无色气体 |
20.下列叙述正确的是( )
| A. | 通常情况下,1.5molO2的体积约为33.6L | |
| B. | NaOH的摩尔质量是40g | |
| C. | 100 mL水中溶解5.85gNaCl所得NaCl溶液的物质的量浓度为1 mol•L-1 | |
| D. | 任何条件下,等物质的量的水和一氧化碳所含有的分子数必相等 |
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: