题目内容
8.在NaOH溶液中通人少量的CO2时,发生反应:2NaOH+CO2═Na2CO2+H2O,而在NaOH溶液中通人过量的CO2时,则发生反应:NaOH+CO2=NaHCO3,现在用1L1.0mo1•L-11a0H溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约是( )| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
分析 根据n=cV计算出氢氧化钠的物质的量,根据反应方程式2NaOH+CO2═Na2CO3+H2O、NaOH+CO2=NaHCO3判断过量情况及反应产物,然后设出未知数计算出Na2CO3和NaHCO3的物质的量的比即可.
解答 解:1L 1.0mol/L 的NaOH溶液中含有氢氧化钠的物质的量为:1mol/L×1L=1mol,
根据2NaOH+CO2═Na2CO3+H2O可知,如果完全反应生成碳酸钠,需要消耗0.5mol二氧化碳,
若生成碳酸氢钠:NaOH+CO2=NaHCO3,则消耗1mol二氧化碳,
所以二者反应生成碳酸钠和碳酸氢钠的混合物,
设反应生成碳酸钠xmol、碳酸氢钠ymol,
则:2x+y=1mol、x+y=0.8mol,
解得:x=0.2mol、y=0.6mol,
则则所得溶液中Na2CO3和NaHCO3的物质的量的比为:0.2mol:0.6mol=1:3,
故选A.
点评 本题考查了化学方程式的计算,题目难度不大,注意根据反应物的物质的量先判断过量情况,从而得出反应产物,然后根据质量守恒定律列式计算,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
19.常温下,pH相同且都等于2的盐酸和醋酸,各取20mL,则下列说法正确的是( )
| A. | 将两种溶液都稀释100倍,醋酸的pH大于盐酸 | |
| B. | 用相同浓度的氢氧化钠溶液中和,消耗氢氧化钠的体积相等 | |
| C. | 分别加入质量相同的足量锌粉,开始时盐酸反应速率快 | |
| D. | 盐酸的浓度为0.01mol•L-1,醋酸浓度大于0.01mol•L-1 |
3.化学与人类生产和生活密切相关,下列说法正确的是( )
| A. | 聚乙烯塑料的老化是由于发生了加成反应 | |
| B. | 加碘食盐中加入的I2有利于防止地方缺碘病 | |
| C. | 二氧化硫有漂白性,常用作棉、麻、纸张的漂白 | |
| D. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 |
13.现有50mL0.1mol•L-1三种一元弱酸,分别用0.1mol•L-1的NaOH溶液滴定,所得滴定曲线如图所示,下列说法正确的是( )
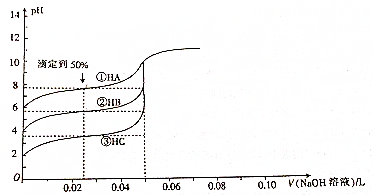

| A. | Ka(HA)>Ka(HB)>Ka(HC) | |
| B. | 滴定到50%时,溶液中:c(A-)>(B-)>(C-) | |
| C. | V(NaOH)溶液=50mL时,溶液中水的电离程度:①>②>③ | |
| D. | V(NaOH)溶液=50mL时,溶液pH的大小关系:pH(A)<pH(B)<pH(C) |
1. 氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位、工业制硝酸的主要反应之一是:
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位、工业制硝酸的主要反应之一是:
(1)如果将4mol NH3 和5mol O2放入容器中,达到平衡时放出热量0.8akJ,则平衡时NH3的转化率为80%.
4NH2(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ•mol-1(a>0)
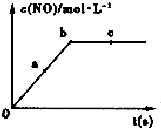
(2)在一定条件下,容积固定的密闭容器中进行上述反应,NO的浓度与时间关系如图所示,则NO的a、b、c三点的反应速率v(a 正)、v(b 逆)、v(c 正)的大小关系是v(a正)>v(b逆)=v(c正).
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如表:
①第2min 到第4min,反应速率v(O2)=0.75mol/(L.min);
②第2min 时改变了条件,改变的条件可能是D(从所给选项中选择);
A.降低温度 B.增加了生成物 C.减小压强 D.使用了高效催化剂
③在与第4min 相同的温度下,若起始向容器中加入NH3、O2、NO 和H2O(g)的浓度都为2moI/L,则该反应正反应方向进行(填“正反应方向进行”、“逆反应方向进行”、“不移动”).
(4)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气.尿素(H2NCONH2)是一种非常重要的高氮化肥,在温度70-95℃时,工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2,尿素与NO、NO2三者等物质的量反应的化学方程式为CO(NH2)2+NO+NO2$\frac{\underline{\;70-95℃\;}}{\;}$N2+CO2+2H2O.
(5)目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kj•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kj•mol-1
则1mol 甲烷直接将NO2 还原为N2的焓变为△H=-867kJ•mol-1.
 氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位、工业制硝酸的主要反应之一是:
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位、工业制硝酸的主要反应之一是:(1)如果将4mol NH3 和5mol O2放入容器中,达到平衡时放出热量0.8akJ,则平衡时NH3的转化率为80%.
4NH2(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ•mol-1(a>0)
(2)在一定条件下,容积固定的密闭容器中进行上述反应,NO的浓度与时间关系如图所示,则NO的a、b、c三点的反应速率v(a 正)、v(b 逆)、v(c 正)的大小关系是v(a正)>v(b逆)=v(c正).
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如表:
| 深度/mol•L-1 时间/min | C(NH3) | c(O2) | c(NO) | c(H2O) |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | 4.5 | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
②第2min 时改变了条件,改变的条件可能是D(从所给选项中选择);
A.降低温度 B.增加了生成物 C.减小压强 D.使用了高效催化剂
③在与第4min 相同的温度下,若起始向容器中加入NH3、O2、NO 和H2O(g)的浓度都为2moI/L,则该反应正反应方向进行(填“正反应方向进行”、“逆反应方向进行”、“不移动”).
(4)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气.尿素(H2NCONH2)是一种非常重要的高氮化肥,在温度70-95℃时,工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2,尿素与NO、NO2三者等物质的量反应的化学方程式为CO(NH2)2+NO+NO2$\frac{\underline{\;70-95℃\;}}{\;}$N2+CO2+2H2O.
(5)目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kj•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kj•mol-1
则1mol 甲烷直接将NO2 还原为N2的焓变为△H=-867kJ•mol-1.
18.第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物
(1)下列叙述正确的是AD
A.HCHO与水分子之间能形成氢键
B.HCHO和CO2分子中的中心原子均采用SP2杂化
C.苯分子中含有6个σ键和1个大π键,苯是非极性分子
D.CO2晶体的熔点、沸点比二氧化硅晶体的低
(2)Mn和Fe部分电力能数据如表:
Mn元素的价电子排布式为3d54s2,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少
(3)铁原子核外有26种运动状态不同的电子.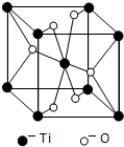
(4)根据元素电子的外围电子排布的特征,可将元素周期表分成五个区域,其中Ti属于d区
(5)Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为TiO2
(6)电镀厂排放的废水中常含有剧毒的CN-离子.可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2
①H、C、N、O四种元素的电负性由小到大的顺序为H<C<N<O
②与CNO-互为等电子体微粒的化学式为CO2、N2O、SCN-等(写一种即可)
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,写出氰酸的结构式:N≡C-O-H.
(1)下列叙述正确的是AD
A.HCHO与水分子之间能形成氢键
B.HCHO和CO2分子中的中心原子均采用SP2杂化
C.苯分子中含有6个σ键和1个大π键,苯是非极性分子
D.CO2晶体的熔点、沸点比二氧化硅晶体的低
(2)Mn和Fe部分电力能数据如表:
| 元素 | Mn | Fe | |
| 电离能/mol | I1 | 717 | 758 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(3)铁原子核外有26种运动状态不同的电子.

(4)根据元素电子的外围电子排布的特征,可将元素周期表分成五个区域,其中Ti属于d区
(5)Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为TiO2
(6)电镀厂排放的废水中常含有剧毒的CN-离子.可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2
①H、C、N、O四种元素的电负性由小到大的顺序为H<C<N<O
②与CNO-互为等电子体微粒的化学式为CO2、N2O、SCN-等(写一种即可)
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,写出氰酸的结构式:N≡C-O-H.
19.现某溶液中可能含有下列6种离子中的某几种:Na+、NH4+、K+、Cl-、SO42-、CO32-.为确认溶液组成进行如下实验:
(1)取200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶.
(2)向(1)所得滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出).
由此可以得出关于原溶液组成的正确结论是( )
(1)取200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶.
(2)向(1)所得滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出).
由此可以得出关于原溶液组成的正确结论是( )
| A. | 一定存在SO42-、CO32-、NH4+,可能存在K+、Cl-、Na+ | |
| B. | 一定存在SO42-、CO32-、NH4+、Cl-,一定不存在K+、Na+ | |
| C. | c(CO32-)=0.01 mol•L-1,c(NH4+)>c(SO42-) | |
| D. | 如果上述6种离子都存在,则c(Cl-)>c(SO42-) |