题目内容
6.如何将30.0g蔗糖(C12H22O11)配制成下列水溶液?(1)糖的质量分数为0.1?
(2)糖的摩尔分数为0.01?
(3)糖的物质的量浓度为0.1mol•L-1?
(4)糖的质量摩尔浓度为0.1mol•Kg-1?
(5)糖的质量浓度为0.1g•L-1?
分析 (1)依据质量分数=$\frac{溶质的质量}{溶液的质量}$×100%解答;
(2)糖的摩尔分数=$\frac{蔗糖的物质的量}{蔗糖物质的量+水分子的物质的量}$×100%;
(3)依据C=$\frac{n}{V}$进行计算;
(4)依据质量摩尔浓度=$\frac{溶质的物质的量}{溶液的质量}$计算;
(5)质量浓度=$\frac{溶质的质量}{溶液的体积}$.
解答 解:(1)将30.0g蔗糖(C12H22O11)配制成质量分数为0.1,设需要加水mg,则$\frac{30.0g}{30.0g+mg}$=0.1,解得m=270.0g;
答:需要加入水270.0g;
(2)30.0g蔗糖的物质的量为:$\frac{30.0g}{342g/mol}$=0.088mol,将30.0g蔗糖(C12H22O11)配制成质量分数为0.1,设需要加水物质的量为nmol,则$\frac{0.088mol}{0.088mol+n}$=0.1,解得n=0.792mol;
答:需要加水0.792mol;
(3)30.0g蔗糖的物质的量为:$\frac{30.0g}{342g/mol}$=0.088mol,要使物质的量浓度为0.1mol•L-1,设溶液体积为V,则$\frac{0.088mol}{V}$=0.1mol•L-1,解得V=0.88L,
答:需要加水使配成的溶液体积为0.088L;
(4)30.0g蔗糖的物质的量为:$\frac{30.0g}{342g/mol}$=0.088mol,要使糖的质量摩尔浓度为0.1mol•Kg-1,设需要加水的质量为mkg,则$\frac{0.088mol}{0.03kg+mkg}$=0.1mol•Kg-1,解得m=
0.85kg;
答:需要加水质量0.85kg;’
(5)将30.0g蔗糖(C12H22O11)配制糖的质量浓度为0.1g•L-1,设配制溶液体积为VL,则$\frac{30.0g}{V}$=0.1g•L-1,解得V=300L,
答:需要加水使配成溶液体积为300L.
点评 本题考查了有关浓度的计算,明确各种浓度的含义及计算公式是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案①取代反应;②加成反应;③使溴水褪色;④使酸性KMnO4溶液褪色;⑤与AgNO3溶液生成白色沉淀;⑥聚合反应.
| A. | 以上反应均可发生 | B. | 只有⑤不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有①不能发生 |
| A. | c(H+)=c(OH-) | B. | c(OH-)>c(H+) | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COOH)+c(CH3COO-)=0.02mol/L |
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 氢氧化铝可作抗酸药 | |
| C. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| D. | 硅胶可用作食品干燥剂 |
| A. | 我国目前最主要的能源是煤炭 | |
| B. | 人类目前所直接利用的能源大部分是由化学反应产生的 | |
| C. | 人体运动所消耗的能量与化学反应无关 | |
| D. | 煤、石油、天然气是当今世界最重要的三种化石原料 |
| A. | ③④⑧ | B. | ④⑤⑧ | C. | ③④⑤ | D. | ④⑤⑦⑧ |
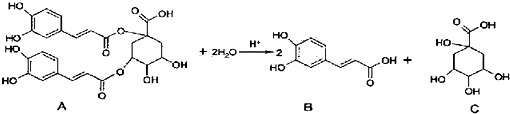
下列说法正确的是( )
| A. | B中共面的原子个数最多为20个 | |
| B. | 1mol A 和足量NaOH 溶液反应,最多消耗11molNaOH | |
| C. | B 能和浓溴水发生反应,1mol B最多消耗4 molBr2 | |
| D. | A、C分子中手性碳原子个数相同 |
| A. | Al(OH)3分解的产物可用于制备金属铝 | |
| B. | 电解熔融氯化钠所得到的金属钠呈液态 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 电解MgCl2水溶液,可制得金属镁 |