题目内容
如何减少汽车等机动车尾气对大气的污染?写出有关反应的化学方程式.
考点:常见的生活环境的污染及治理
专题:
分析:根据动车排放的尾气的成分中常含有NO、CO等气体分析.
解答:
解:机动车排放的尾气中常含有NO、CO和CO2等气体,如果在汽车上装一个尾气处理装置,在催化剂的作用下,使NO和CO发生反应,生成氮气和二氧化碳,该反应的化学方程式 2NO+2CO
N2+2CO2;
故答案为:2NO+2CO
N2+2CO2.
| ||
故答案为:2NO+2CO
| ||
点评:本题难度不大,理解题意、掌握空气的污染原因和治理是正确解答本题的关键.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
制备氰氨化钙的化学方程式为CaCO3+2HCN═CaCN2+CO↑+H2↑+CO2↑,在反应中( )
①氢元素被氧化,碳元素被还原
②HCN既是氧化剂又是还原剂
③CaCN2是氧化产物,H2是还原产物
④CO为氧化产物,H2为还原产物.
①氢元素被氧化,碳元素被还原
②HCN既是氧化剂又是还原剂
③CaCN2是氧化产物,H2是还原产物
④CO为氧化产物,H2为还原产物.
| A、①② | B、③④ | C、①④ | D、②③ |
在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2中,若有5mol水发生氧化反应,则被还原的BrF3物质的量为( )
| A、2mol | ||
B、
| ||
C、
| ||
| D、5mol |
下列说法正确的是( )
| A、CS2为V形的极性分子 |
| B、电子云示意图中的每个小黑点都表示一个电子 |
| C、非极性键也可以存在于化合物中 |
| D、甲烷、氨和水都是由极性键结合而成的极性分子 |
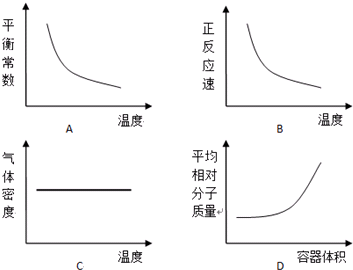
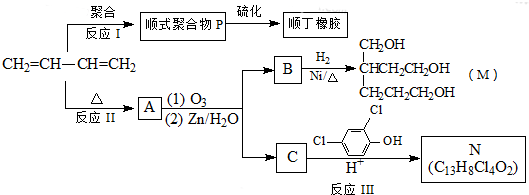
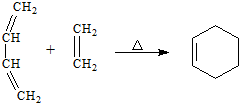
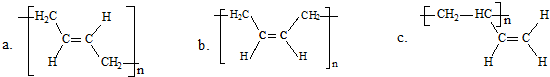
 二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)以其优良的性质,被称为21世纪的新型“清洁能源”,在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以C0和H2为原料生产CH30CH3的新工艺主要发生三个反应: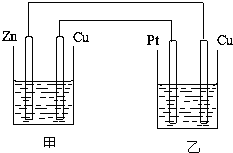 如图所示的装置,甲装置中的电解质溶液为硫酸铜溶液,乙中为稀硫酸,请按以下要求回答问题.
如图所示的装置,甲装置中的电解质溶液为硫酸铜溶液,乙中为稀硫酸,请按以下要求回答问题.