题目内容
18.FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断正确的是( )| A. | 溶液中一定含Cu2+ | B. | 溶液中不一定含Fe2+ | ||
| C. | 剩余固体一定含Cu和Fe | D. | 加入KSCN溶液一定不变红色 |
分析 Fe3+、Cu2+的氧化性强弱为:Fe3+>Cu2+,Fe3+优先反应,固体有剩余,则反应后的溶液中一定不存在Fe3+;若剩余固体只有Cu,则反应后的溶液中一定Fe3+存在,一定存在Fe2+,可能含有Cu2+;若有Fe剩余,一定有铜生成,Fe3+和Cu2+无剩余,据此进行判断.
解答 解:①当固体为铁、铜时,溶液中的Fe3+、Cu2+全部参加反应生成Fe2+和Cu,反应的方程式为:2FeCl3+Fe=3FeCl2、CuCl2+Fe=Cu+FeCl2,所以溶液中一定没有Fe3+、Cu2+,一定含有Fe2+;
②当固体为铜时,溶液中一定没有Fe3+,Cu2+恰好全部参加反应或部分反应生成Fe2+和Cu,所以溶液中一定没有Fe3+,可能含有Cu2+,一定含有Fe2+;
A、若有Fe剩余,一定有铜生成,Fe3+和Cu2+无剩余,故A错误;
B、固体有剩余,Fe3+、Cu2+的氧化性强弱为:Fe3+>Cu2+,Fe3+优先反应,溶液中一定存在Fe2+,故B错误;
C、若铁过量,剩余的固体为铜和铁的混合物,故C错误;
D、由于金属有剩余,溶液中一定不存在Fe3+,所以加入KSCN溶液一定不变红色,故D正确;
故选D.
点评 本题考查了Fe3+、Cu2+的氧化能力大小的比较,题目难度中等,正确判断Fe3+、Cu2+的氧化性强弱及固体的成分是解本题的关键,注意掌握铁离子与金属铜、铁反应的化学方程式.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
9.两种金属A与B和稀硫酸组成原电池时,A是正极.下列有关推断正确的是( )
| A. | A的金属性强于B | |
| B. | 电子不断由A电极经外电路流向B电极 | |
| C. | A电极上发生的电极反应是还原反应 | |
| D. | A的金属活动性一定排在氢前面 |
13.关于浓度均为0.1mol•L-1的三种溶液:①醋酸溶液 ②NaOH溶液 ③醋酸钠溶液,下列说法不正确的是( )
| A. | c(CH3COO-):③>① | |
| B. | 水电离出的c(OH-):②>① | |
| C. | ①和②等体积混合后的溶液:c(OH-)=c(H+)+c(CH3COOH) | |
| D. | ①和③等体积混合后的溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
3.下列的一些说法,不正确的有( )
①焰色反应是化学变化;
②干馏和分馏都属于化学变化;
③单质钠加入氯化镁溶液中制取镁;
④可以用电解熔融的氯化钠的方法来制取金属钠;
⑤用电解法制铝时,原料是氯化铝
⑥石英、玛瑙、水晶、玻璃、水泥、陶瓷、太阳能电池和光纤都是硅酸盐产品.
①焰色反应是化学变化;
②干馏和分馏都属于化学变化;
③单质钠加入氯化镁溶液中制取镁;
④可以用电解熔融的氯化钠的方法来制取金属钠;
⑤用电解法制铝时,原料是氯化铝
⑥石英、玛瑙、水晶、玻璃、水泥、陶瓷、太阳能电池和光纤都是硅酸盐产品.
| A. | ②③④⑤ | B. | ①③⑤⑥ | C. | ①②③⑤⑥ | D. | ①②③④⑤⑥ |
10.图分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中正确的是( )


| A. | 金刚石转变为石墨是吸热反应 | |
| B. | S(g)+O2(g)═SO2(g)△H1,S(s)+O2(g)═SO2(g)△H2,则△H1>△H2 | |
| C. | 白磷比红磷稳定 | |
| D. | CO(g)+H2O(g)═CO2(g)+H2(g)△H<0 |
7. 化学反应过程中发生物质变化的同时,常常伴有能量的变化,这种能量的变化常以热能的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
化学反应过程中发生物质变化的同时,常常伴有能量的变化,这种能量的变化常以热能的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
(1)下列△H表示物质燃烧热的是△H4、△H5;表示物质中和热的是△H6.(填“△H1”、“△H2”和“△H3”等)
A.2H2(g)+O2(g)=2H2O(l)△H1
B.C(s)+1/2O2(g)=CO(g)△H2
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)=CO2(g)△H4
E.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H7
(2)已知在101kPa、273K时,15g乙烷燃烧生成CO2和液态水,放出akJ的热量,下列热化学方程式正确的是C.
A.C2H6(g)+$\frac{7}{2}$O2(g)=2CO2(g)+3H2O(l)△H=+2akJ/mol
B.C2H6(g)+$\frac{7}{2}$/2O2(g)=2CO2(g)+3H2O(g)△H=-2akJ/mol
C.2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l)△H=-4akJ/mol
D.2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g)△H=-4akJ/mol
(3)进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关(键能可以简单地理解为断开1mol化学键时所需吸收的能量),如表是部分化学键的键能数据:
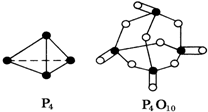
已知白磷(P4)的燃烧热为2378.0kJ/mol,白磷完全燃烧的产物(P4O10)的结构如图所示,则如表中a=433.75.
(4)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ/mol.
 化学反应过程中发生物质变化的同时,常常伴有能量的变化,这种能量的变化常以热能的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
化学反应过程中发生物质变化的同时,常常伴有能量的变化,这种能量的变化常以热能的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.(1)下列△H表示物质燃烧热的是△H4、△H5;表示物质中和热的是△H6.(填“△H1”、“△H2”和“△H3”等)
A.2H2(g)+O2(g)=2H2O(l)△H1
B.C(s)+1/2O2(g)=CO(g)△H2
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)=CO2(g)△H4
E.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H7
(2)已知在101kPa、273K时,15g乙烷燃烧生成CO2和液态水,放出akJ的热量,下列热化学方程式正确的是C.
A.C2H6(g)+$\frac{7}{2}$O2(g)=2CO2(g)+3H2O(l)△H=+2akJ/mol
B.C2H6(g)+$\frac{7}{2}$/2O2(g)=2CO2(g)+3H2O(g)△H=-2akJ/mol
C.2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l)△H=-4akJ/mol
D.2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g)△H=-4akJ/mol
(3)进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关(键能可以简单地理解为断开1mol化学键时所需吸收的能量),如表是部分化学键的键能数据:
| 化学键 | P-P | P-O | O═O | P═O |
| 键能KJ/mol | 197 | 360 | 499 | a |
(4)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ/mol.
8.下列化学用语书写正确的是( )
| A. | 乙酸乙酯的结构简式:CH3CH2COOCH3 | |
| B. | 丙烯的键线式 | |
| C. | 乙醇的结构式: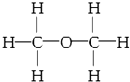 | |
| D. | 乙烯的结构简式:CH2=CH2 |
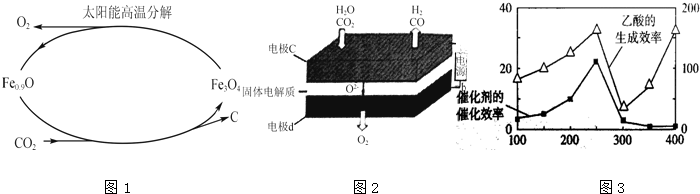
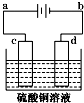 粗铜的电解精炼如图所示.在粗铜的电解过程中,粗铜板应是图中电极c(填图中的字母);在电极d上发生的电极反应式为Cu2++2e-═Cu.
粗铜的电解精炼如图所示.在粗铜的电解过程中,粗铜板应是图中电极c(填图中的字母);在电极d上发生的电极反应式为Cu2++2e-═Cu.