题目内容
6.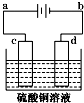 粗铜的电解精炼如图所示.在粗铜的电解过程中,粗铜板应是图中电极c(填图中的字母);在电极d上发生的电极反应式为Cu2++2e-═Cu.
粗铜的电解精炼如图所示.在粗铜的电解过程中,粗铜板应是图中电极c(填图中的字母);在电极d上发生的电极反应式为Cu2++2e-═Cu.
分析 用电解法进行粗铜提纯时,粗铜应作阳极,精铜作阴极;阳极与电池的正极相连发生氧化反应,阴极与电池的负极相连发生还原反应,据此分析.
解答 解:用电解法进行粗铜提纯时,粗铜应作阳极,精铜作阴极;
该装置中a为原电池的正极,b为原电池的负极,所以c为电解池的阳极,d为电解池的阴极,电解时,以硫酸铜溶液为电解液,溶液中的Cu2+得到电子沉积在阴极上,发生还原反应,即d电极上发生的反应为:Cu2++2e-=Cu;
故答案为:c;Cu2++2e-═Cu.
点评 本题考查铜的电解精炼,题目难度不大,注意把握电解池中阴阳极的判断以及电极方程式的书写,侧重于考查学生的分析能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
17.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
| A. | Na2CO3和Na2O2都属于盐 | B. | KOH和KHCO3都属于碱 | ||
| C. | H2SO4和H3PO4都属于酸 | D. | Na2O和Na2SiO3都属于氧化物 |
14.盐A与酸B反应,可放出有气味的气体C,C与NaOH反应生成A;C最终可氧化生成D;D溶于水生成B,则A、B分别是( )
| A. | Na2S和HCl | B. | Na2S和H2SO4 | C. | Na2SO3和HCl | D. | Na2SO3和H2SO4 |
11.某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M,经测定Fe3+、SO42-、Al3+和M的物质的量之比为2:4:1:1,则M可能是下列中的( )
| A. | Na+ | B. | OH- | C. | Cl- | D. | S2- |
18.FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断正确的是( )
| A. | 溶液中一定含Cu2+ | B. | 溶液中不一定含Fe2+ | ||
| C. | 剩余固体一定含Cu和Fe | D. | 加入KSCN溶液一定不变红色 |
15.短周期主族元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为18.X与Y、Z位于相邻周期,Y原子最外层电子数是X原子内层电子数的3倍,下列说法正确的是( )
| A. | Y的低价氧化物能使Z单质的水溶液褪色 | |
| B. | X的氢化物溶于水显酸性 | |
| C. | 其离子半径大小:Z>Y>X | |
| D. | X的氢化物和Z的最高价氧化物对应的水化物不能反应生成盐 |
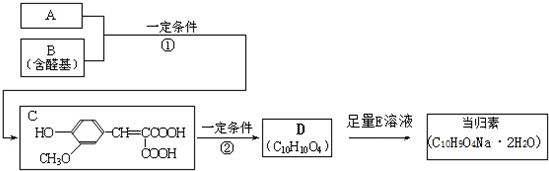
 .
. .
.