题目内容
下列关于胶体的认识错误的是( )
| A、将含0.1mol/L的氯化铁饱和溶液滴入沸水中形成的胶体粒子数目小于0.1NA |
| B、纳米材料微粒直径一般从几纳米到几十纳米.因此纳米材料属于胶体 |
| C、往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 |
| D、水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷 |
考点:胶体的重要性质
专题:溶液和胶体专题
分析:A.胶体微粒是氢氧化铁的集合体,溶液体积不知不能计算微粒数进行判断;
B.纳米材料不是分散系;
C.胶体遇电解质发生聚沉;
D.如果悬浮液中不同物质荷电情况不同,那可以通过电泳方式分离.
B.纳米材料不是分散系;
C.胶体遇电解质发生聚沉;
D.如果悬浮液中不同物质荷电情况不同,那可以通过电泳方式分离.
解答:
解:A.胶体微粒是氢氧化铁的集合体,将含0.1mol/L的氯化铁饱和溶液滴入沸水中,溶液体积不知,形成的胶体粒子数目不能确定小于0.1NA ,故A错误;
B.纳米材料只是一种分散质,没有形成体系,所以不是胶体,故B错误;
C.胶体遇电解质发生聚沉,氢氧化铁沉淀可溶于硫酸,故C正确;
D.因为电泳的原理就是电场驱动带电颗粒的移动,如果悬浮液中不同物质荷电情况不同,那可以通过电泳方式分离,水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷,故D正确.
故选AB.
B.纳米材料只是一种分散质,没有形成体系,所以不是胶体,故B错误;
C.胶体遇电解质发生聚沉,氢氧化铁沉淀可溶于硫酸,故C正确;
D.因为电泳的原理就是电场驱动带电颗粒的移动,如果悬浮液中不同物质荷电情况不同,那可以通过电泳方式分离,水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷,故D正确.
故选AB.
点评:本题考查胶体的性质,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列关于镁及其化合物的叙述不正确的是( )
| A、把镁粉投入氯化铁溶液中,常温下不会有氢气放出 |
| B、工业上通常用煅烧菱镁矿来制取氧化镁 |
| C、镁的主要用途是用于制造合金和照明弹 |
| D、食盐中如含氯化镁就易潮解 |
随着矿石能源的紧缺,电动汽车将成为汽车市场的主角.电动汽车以LiFePO4电池作为动力,LiFePO4电池具有稳定性高、安全、对环境友好等优点.电池反应为:LiFePO4
FePO4+Li,负极材料是石墨,电解质为含Li+的导电固体.下列有关LiFePO4电池说法正确的是( )
| 充电 |
| 放电 |
| A、放电时电池内部Li+向负极移动 |
| B、电池的负材料为Li |
| C、放电过程中,电池正极材料发生氧化反应 |
| D、充电时阴极反应为:FePO4+Li++e-═LiFePO4 |
阿伏加德罗常数用NA表示,下列叙述正确的是( )
| A、常温常压下,1 mol NO2中含有的分子数为 NA |
| B、常温常压下,0.2mol铁在0.2 mol氯气中充分燃烧,转移的电子数为 0.6NA |
| C、7.8g过氧化钠粉末与足量二氧化硫反应转移的电子数为0.2NA |
| D、11.2L Cl2通入足量氢氧化钠溶液中充分反应,转移的电子数为0.5NA |
下列反应的离子方程式书写正确的是( )
| A、钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ |
| B、金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-+H2↑ |
| C、向Al2(SO4)3溶液中加入过量的氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| D、少量SO2通入漂白粉溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO |
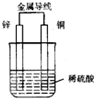 如图是铜锌原电池,某同学做完实验后记录如下:
如图是铜锌原电池,某同学做完实验后记录如下: