题目内容
17.下列各表述与如图所示一致的是( )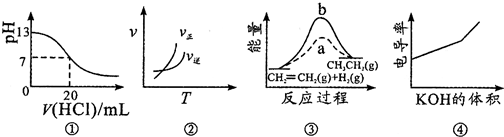
| A. | 图①表示25℃时,用0.1mol•L-1盐酸滴定20mL0.1mol•L-1NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应A2(g)+3B2(g)?2AB3(g)△H<0 | |
| C. | 图③中a、b曲线分别表示反应CH2═CH2(g)+H2(g)═CH3CH3(g)△H<0,使用和未使用催化剂时反应过程中的能量变化 | |
| D. | 电导率是衡量电解质溶液导电能力大小的物理量,图④表示KOH溶液滴定CH3COOH溶液时溶液的电导率变化曲线示意图 |
分析 A、酸碱中和的时候pH会突变;
B、对于可逆反应A2(g)+3B2(g)?2AB3(g)(△H<0),反应放热,升高温度,正逆反应速率都增大,平衡向逆反应方向移动;
C、图象中使用催化剂降低反应活化能,但反应是放热反应,反应物能量高;
D、溶液导电能力与离子浓度成正比,CH3COOH是弱电解质,溶液中离子浓度较小,加入KOH后,溶液中离子浓度增大,溶液导电性增强.
解答 解:A、用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1NaOH溶液的pH随加入盐酸体积的变化,pH会突变,故A错误;
B、反应放热,升高温度,正逆反应速率都增大,正反应速率增大的倍数比逆反应速率小,平衡向逆反应方向移动,故B错误;
C、图象中使用催化剂降低反应活化能,但反应是放热反应,反应物能量高,图象中表示的吸热反应,故C错误;
D、溶液导电能力与离子浓度成正比,CH3COOH是弱电解质,溶液中离子浓度较小,加入KOH后,溶液中离子浓度增大,溶液导电性增强,故D正确;
故选D.
点评 本题考查了化学反应能量变化,影响溶液导电性判断,图象分析方法和平衡移动原理的判断依据是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列反应中,水作氧化剂的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 2Na2O2+2H2O═4NaOH+O2↑ | ||
| C. | CuO+H2 $\frac{\underline{\;高温\;}}{\;}$ Cu+H2O | D. | Na2O+H2O═2NaOH |
8.世界上一次性建成的最长高速铁路--京沪高铁,列车时速高达380公里,车厢大部分采用铝合金材料制造,这是因为铝合金( )
| A. | 比纯铝熔点高 | |
| B. | 各种成分在自然界中含量丰富,容易获取 | |
| C. | 具有比较活泼的化学性质 | |
| D. | 质量轻,强度大,抗腐蚀能力比较强 |
5.下列反应中不是氧化还原反应的是( )
| A. | 3Cl2+6KOH═5KCl+KClO3+3H2O | B. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2AgNO3+BaCl2═2AgCl↓+Ba(NO3)2 |
12.如表是元素周期表的一部分.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
(1)写出下列元素符号:①N,⑥Si.
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程: .
.
(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是H2S.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程:
 .
.(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是H2S.
2.烷烃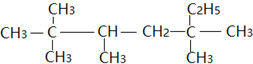 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
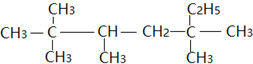 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
9.欲制取较纯净的CH2ClCH2Cl,可采取的方法是( )
| A. | 乙烷与Cl2取代 | B. | 乙烯与Cl2加成 | ||
| C. | 乙醇与浓盐酸取代 | D. | 乙炔与HCl加成 |
 ,则合成涤纶的反应方程式和反应类型分别是
,则合成涤纶的反应方程式和反应类型分别是 、缩聚反应.
、缩聚反应.