题目内容
取未知浓度的硫酸10.0mL,进行中和滴定,当滴入25.0mLNaOH溶液时,发觉已过量.再用1.00mol/L的盐酸回滴,加入5.0mL正好中和过量的碱.已知同样浓度的盐酸中和10.0mL上述NaOH溶液,消耗盐酸24.0mL.求原硫酸的物质的量浓度.
考点:物质的量浓度的相关计算
专题:
分析:发生反应的实质为H++OH-=H2O,反应满足关系n(H+)=n(OH-),以此计算该题.
解答:
解:发生反应的实质为H++OH-=H2O,
令硫酸的浓度为c,取未知浓度的硫酸10.0mL,进行中和滴定,当滴入25.0mLNaOH溶液时,发觉已过量.再用1.00mol/L的盐酸回滴,加入5.0mL正好中和过量的碱,则应有0.01L×2×c+0.005L×1.00mol/L=0.025L×c(NaOH),
而已知同样浓度的盐酸中和10.0mL上述NaOH溶液,消耗盐酸24.0mL,则0.024L×1.00mol/L=0.01L×c(NaOH),c(NaOH)=2.4mol/L,
所以0.01L×2×c=0.025L×2.4L/mol-0.05L×1.00L/mol=0.01mol,
c=0.5mol/L,
答:原硫酸的物质的量浓度为0.5mol/L.
令硫酸的浓度为c,取未知浓度的硫酸10.0mL,进行中和滴定,当滴入25.0mLNaOH溶液时,发觉已过量.再用1.00mol/L的盐酸回滴,加入5.0mL正好中和过量的碱,则应有0.01L×2×c+0.005L×1.00mol/L=0.025L×c(NaOH),
而已知同样浓度的盐酸中和10.0mL上述NaOH溶液,消耗盐酸24.0mL,则0.024L×1.00mol/L=0.01L×c(NaOH),c(NaOH)=2.4mol/L,
所以0.01L×2×c=0.025L×2.4L/mol-0.05L×1.00L/mol=0.01mol,
c=0.5mol/L,
答:原硫酸的物质的量浓度为0.5mol/L.
点评:本题考查物质的量浓度的计算,侧重于学生的分析能力和计算能力的考查,注意把握反应的关系,难度不大.

练习册系列答案
相关题目
如图有关电化学的示意图正确的是( )
A、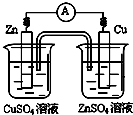 |
B、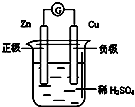 |
C、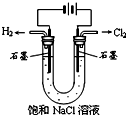 |
D、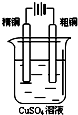 |
当今国际能源研究的热点之一是寻找新能源,下列能源不属于新能源的是( )
| A、太阳能 | B、氢能 |
| C、地热能 | D、水能 |
下列反应属于吸热反应的是( )
| A、铝热反应 |
| B、酸碱中和反应 |
| C、锌粒与稀硫酸反应制取H2 |
| D、Ba(OH)2?8H2O与NH4Cl反应 |
下列关于氧化还原反应的说法正确的是( )
| A、氧化还原反应中,发生氧化还原的一定是不同种元素 |
| B、氧化剂和还原剂一定是不同种物质 |
| C、还原剂失去电子总数一定等于氧化剂得到电子总数 |
| D、某氧化还原反应中,还原剂共失去4e-,氧化剂共得到4e-,所以该反应转移的电子总数为8e- |