题目内容
.为除去粗盐中的Ca2+、Mg2+、Fe3+、SO
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)判断BaCl2已过量的方法是 .
(2)第④步中,相关的化学方程式是 .
(3)配制NaCl溶液时,若出现下列操作,其结果怎样?在下列括号中填写“偏高”、“偏低”或“不变”.
A.称量时NaCl已潮解
B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水
D.定容时俯视刻度线
E.容量瓶用蒸馏水洗净后未干燥 .
2- 4 |

(1)判断BaCl2已过量的方法是
(2)第④步中,相关的化学方程式是
(3)配制NaCl溶液时,若出现下列操作,其结果怎样?在下列括号中填写“偏高”、“偏低”或“不变”.
A.称量时NaCl已潮解
B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水
D.定容时俯视刻度线
E.容量瓶用蒸馏水洗净后未干燥
考点:粗盐提纯
专题:实验设计题
分析:(1)根据钡离子能和硫酸根之间反应生成硫酸钡沉淀来检验氯化钡是否过量;
(2)碳酸钠可以将钙离子以及过量的钡离子沉淀下来;
(3)分析具体操作对m、V的影响,根据c=
=
分析不当操作对溶液浓度的影响.
(2)碳酸钠可以将钙离子以及过量的钡离子沉淀下来;
(3)分析具体操作对m、V的影响,根据c=
| n |
| V |
| m |
| MV |
解答:
解:(1)过量的氯化钡会将全部的硫酸根离子沉淀完毕,只要是硫酸根剩余,则氯化钡会与其反应出现白色沉淀,所以判断BaCl2已过量的方法是:取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量,
故答案为:取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量;
(2)碳酸钠可以将钙离子以及过量的钡离子沉淀下来,反应原理是Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓,
故答案为:CaCl2+Na2CO3═CaCO3↓+2NaCl,BaCl2+Na2CO3═BaCO3↓+2NaCl;
(3)A.称量时NaCl已潮解,m偏小,则所配溶液浓度偏低,
故答案为:偏低;
B.天平是较精密的测量工具,当砝码生锈时,砝码的质量比所标的值偏大,m偏大,则所配溶液浓度偏高,
故答案为:偏高;
C.定容摇匀时,液面下降又加水,导致所配溶液体积v偏大,所配溶液浓度偏低,
故答案为:偏低;
D.定容时俯视读取刻度,导致所配溶液体积V偏小,所配溶液浓度偏高,
故答案为:偏高.
E、容量瓶是定容仪器,使用时,用蒸馏水洗净后未干燥,不会影响结果,故答案为:不变.
故答案为:取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量;
(2)碳酸钠可以将钙离子以及过量的钡离子沉淀下来,反应原理是Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓,
故答案为:CaCl2+Na2CO3═CaCO3↓+2NaCl,BaCl2+Na2CO3═BaCO3↓+2NaCl;
(3)A.称量时NaCl已潮解,m偏小,则所配溶液浓度偏低,
故答案为:偏低;
B.天平是较精密的测量工具,当砝码生锈时,砝码的质量比所标的值偏大,m偏大,则所配溶液浓度偏高,
故答案为:偏高;
C.定容摇匀时,液面下降又加水,导致所配溶液体积v偏大,所配溶液浓度偏低,
故答案为:偏低;
D.定容时俯视读取刻度,导致所配溶液体积V偏小,所配溶液浓度偏高,
故答案为:偏高.
E、容量瓶是定容仪器,使用时,用蒸馏水洗净后未干燥,不会影响结果,故答案为:不变.
点评:本题考查常见仪器的使用和化学基本操作的方法和误差分析,题目难度不大,注意在学习中加强基础知识的积累.注意根据c=
=
分析分析不当操作对溶液浓度的影响.
| n |
| V |
| m |
| MV |

练习册系列答案
相关题目
下列物质的检验,其结论一定正确的是( )
| A、某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明该溶液中一定含有SO42- |
| B、某溶液中加盐酸产生刺激性气味的无色气体,该气体能使品红溶液褪色,说明该溶液中一定含有SO32- |
| C、某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32- |
| D、取少量久置的Na2SO3样品于试管中加水溶解,再加入足量盐酸有气体产生,然后再加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
下列描述正确的是( )
| A、氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同 |
| B、滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存 |
| C、某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42- |
| D、Fe(N03)2溶液中滴加少量稀硫酸会变黄色 |
如图有关电化学的示意图正确的是( )
A、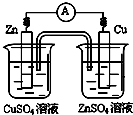 |
B、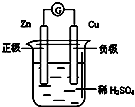 |
C、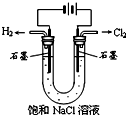 |
D、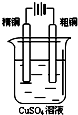 |
 现有FeCl3、FeCl2、CuCl2的混合溶液1L,将0.70mol的铁粉慢慢加入混合液中并充分搅拌,溶液中的三种金属阳离子的物质的量随铁粉加入量的变化曲线如图所示,D点坐标是(0.4,0),H点坐标是(0.7,0.2).
现有FeCl3、FeCl2、CuCl2的混合溶液1L,将0.70mol的铁粉慢慢加入混合液中并充分搅拌,溶液中的三种金属阳离子的物质的量随铁粉加入量的变化曲线如图所示,D点坐标是(0.4,0),H点坐标是(0.7,0.2).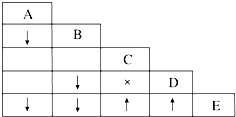 有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.
有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如表所示.表中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做.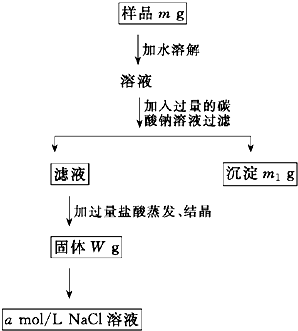 欲用含有少量氯化钙的氯化钠固体,配制100mL a mol/L的氯化钠溶液,设计了下面的操作方案.根据方案操作步骤回答下列问题:
欲用含有少量氯化钙的氯化钠固体,配制100mL a mol/L的氯化钠溶液,设计了下面的操作方案.根据方案操作步骤回答下列问题: