题目内容
7.用惰性电极电解一定浓度的CuSO4溶液,通电一段时间后,向所得溶液中加入0.1mol Cu2(OH)2CO3,溶液恰好恢复到电解前的浓度和pH(不考虑溶液体积变化和CO2溶解造成的影响),则电解过程中转移的电子为( )| A. | 0.4mol | B. | 0.5mol | C. | 0.6mol | D. | 0.8mol |
分析 加入0.1mol Cu2(OH)2CO3能使电解后的溶液恢复原状,加入的 Cu2(OH)2CO3相当于2CuO.H2O.CO2,实际上加入的物质相当于0.1mol (2CuO.H2O),阴极上析出Cu、H2,阳极上只析出O2,根据O原子和转移电子子之间的关系式计算转移电子物质的量.
解答 解:加入0.1mol Cu2(OH)2CO3能使电解后的溶液恢复原状,加入的 Cu2(OH)2CO3相当于2CuO.H2O.CO2,实际上加入的物质相当于0.1mol (2CuO.H2O),阴极上析出Cu、H2,阳极上只析出O2,阳极上转移电子的物质的量=0.1mol×3[0.1mol (2CuO.H2O)中O原子个数]×2=0.6mol,故选C.
点评 本题以物质的量的计算为载体考查电解原理,为高频考点,侧重考查学生分析判断及计算能力,明确“析出什么加入什么”原则是解本题关键,注意各个电极上放电的离子,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.某反应A(g)+B(g)?C(g)的能量变化如图所示,由图象可知,加入X后( )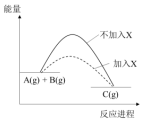

| A. | 反应速率增大 | B. | 反应物转化率增大 | ||
| C. | 生成物的能量降低 | D. | 反应的热效应降低 |
19.下列实验操作能达到实验目的是( )
| A. | 用排水法收集铜粉与浓硝酸反应产生的NO2 | |
| B. | 用氨水鉴别NaCl、MgCl2、AlCl3、NH4Cl四种溶液 | |
| C. | 用酸性KMnO4溶液验证草酸的还原性 | |
| D. | 用饱和NaHCO3溶液除去Cl2中混有的HCl |
16.下列现象中硫酸表现出既有氧化性又有酸性的是( )
| A. | 铜与浓硫酸共热有气体放出 | |
| B. | 用玻璃棒蘸浓硫酸滴在白纸上,白纸变黑 | |
| C. | 把木炭放入热的浓硫酸中,有气体放出 | |
| D. | 常温下可用铁、铝制容器盛装冷的浓硫酸 |
17.下列说法正确的是( )
| A. | 向容量瓶转移液体时,玻璃棒下端伸入到容量瓶刻度线以下 | |
| B. | 用玻璃棒蘸取CH3COOH溶液点在已湿润的pH试纸上,测定该溶液的pH | |
| C. | 用长颈漏斗分离乙酸乙酯和水 | |
| D. | 淀粉溶液与硫酸共热后,加入新制氢氧化铜加热,无砖红色沉淀生成,说明淀粉没有水解 |