题目内容
2.研究氮氧化物反应机理,对于控制汽车尾气、保护环境有重要意义.(1)NO在空气中存在如下反应:2NO(g)+O2(g)?2NO2(g)△H.
上述反应分两步完成,其中第一步反应①如下,写出第二步反应②的热化学方程式(其反应的焓变△H2用含△H、△H1的式子来表示):
①2NO(g)?N2O2(g)△H1<0;
②N2O2(g)+O2(g)=2NO2(g)△H2=△H-△H1 .
上述①反应中,正反应速率为v正=k正c2(NO),逆反应速率为v逆=k逆c(N2O2),其中k正、k逆为速率常数,K为该温度下的平衡常数,则k逆为k正×$\frac{1}{k}$(以K和k正表示).
(2)2NO(g)+O2(g)?2NO2(g)的两步反应中,反应①的反应速率数值较大,是一个快反应,会快速建立平衡状态,而反应②是一个慢反应.反应体系升高温度的过程中,发现2NO(g)+O2(g)?2NO2(g)的反应速率变慢,结合该反应的两步反应过程分析可能的原因决定总反应速率是反应②,温度升高后反应①平衡向左移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢(反应未使用催化剂).
(3)电解法处理氮氧化合物是目前大气污染治理的一个新思路,原理是将NOx在电解池中分解成无污染的N2和O2除去,如图1示,两电极间是新型固体氧化物陶瓷,在一定条件下可自由传导O2-,电解池阴极反应为2NOx+4xe-=N2+2xO2-.
(4)汽车的排气管上装一个“催化转化器”使汽车尾气中的CO和NO发生反应2NO(g)+2CO(g)?2CO2(g)+N2(g)以减 少污染.当质量一定时,增大固体催化剂的表面积可提高化学反应速率.若催化剂的表面积S1>S2,在图2中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线.

分析 (1)第二步反应②为:N2O2(g)+O2(g)?2NO2,根据盖斯定律①+②可得:2NO(g)+O2(g)?2NO2(g),总的热化学方程式-①可得②;可逆反应到达平衡时正逆速率相等;
(2)慢反应决定整个过程的反应速率;决定总反应速率是反应②,温度升高后反应①平衡向右移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢;
(3)电解法处理氮氧化合物原理是将NOx在电解池中分解成无污染的N2和O2除去,两电极间是固体氧化物电解质,在一定条件下可自由传导O2-,阴极发生还原反应,阴极上是NOx获得电子生成N2与O2-;
(4)在2NO(g)+2CO(g)?2CO2(g)+N2(g)的反应体系,当质量一定时,增大固体催化剂的表面积可提高化学反应速率,反应速率加快,缩短到达平衡的时间,不影响平衡移动,平衡时一氧化氮的浓度不变;
解答 解:(1)第二步反应②为:N2O2(g)+O2(g)?2NO2,根据盖斯定律①+②可得:2NO(g)+O2(g)?2NO2(g),总的热化学方程式-①可得②,则反应②的热化学方程式为:N2O2(g)+O2(g)=2NO2(g)△H2=△H-△H1 ,平衡时正逆反应速率相等,k正c2(NO)=k逆c(N2O2),k=$\frac{c({N}_{2}{O}_{2})}{{c}^{2}(NO)}$,k逆=k正×$\frac{1}{k}$
故答案为:N2O2(g)+O2(g)=2NO2(g)△H2=△H-△H1 ;k正×$\frac{1}{k}$;
(2)慢反应决定整个过程的反应速率,决定总反应速率是反应②,温度升高后反应①平衡向右移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢,
故答案为:决定总反应速率是反应②,温度升高后反应①平衡向右移动,造成N2O2浓度减小,温度升高对于反应②的影响弱于N2O2浓度减小的影响,N2O2浓度减小导致反应②速率变慢;
(3)电解法处理氮氧化合物原理是将NOx在电解池中分解成无污染的N2和O2除去,两电极间是固体氧化物电解质,在一定条件下可自由传导O2-,阴极发生还原反应,阴极上是NOx获得电子生成N2与O2-,电极反应式为:2NOx+4xe-=N2+2xO2-,
故答案为:2NOx+4xe-=N2+2xO2-;
(4)在2NO(g)+2CO(g)?2CO2(g)+N2(g)的反应体系,当质量一定时,增大固体催化剂的表面积可提高化学反应速率,反应速率加快,缩短到达平衡的时间,不影响平衡移动,平衡时一氧化氮的浓度不变,在图中画出该反应体系反应进程可能的曲线为: ,
,
故答案为: .
.
点评 本题考查电解原理的分析应用.化学平衡有关计算与影响因素,侧重对化学平衡的影响因素考查,注意化学平衡常数只受温度影响,题目难度较大,答题时注意题中信息的灵活运用.

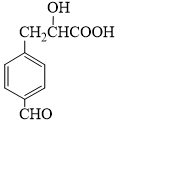
| A. | 能发生缩聚反应 | B. | 能发生消去反应 | ||
| C. | 1mol X最多消耗5 mol H2 | D. | 1mol X最多消耗2 mol Na |
| A. | 20 g D2O 含有的质子数为10NA | |
| B. | 1mol Na2O2与足量水反应转移的电子数为NA,生成的气体在标况下的体积为22.4L | |
| C. | 1L 0.1mol/L HF溶液中含有共价键数目为0.1 NA | |
| D. | NA个Fe(OH)3胶体粒子的质量为107g |
| A. | 粗盐在空气中易潮解 | B. | NH4Cl与ZnCl2用于金属焊接中除锈 | ||
| C. | 用热纯碱溶液去油污 | D. | 蒸干并灼烧FeCl3溶液得到Fe2O3 |
| A. | 0.1molKClO4 | B. | 0.1molKClO3 | C. | 0.2molKClO2 | D. | 0.1molKClO2 |
| A. | 0.4mol | B. | 0.5mol | C. | 0.6mol | D. | 0.8mol |
| A. | 离子半径大小顺序:r(Z2+)>r(Y2-) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | 单质的熔点Z>W |
| A. | 浓硫酸可作干燥剂 | B. | SO2可作食品的漂白剂 | ||
| C. | 漂白液可作环境的消毒剂 | D. | KAl(SO4)2•12H2O可作净水剂 |
| A. | 在熔融状态下,1molNa2O2完全电离出的离子数目为4 NA | |
| B. | 常温下,0.05molCO2和SO2混合气体中所含氧原子数为0.1 NA | |
| C. | 0.1 mol•L-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA | |
| D. | 0.1 mol MnO2与足量的浓盐酸加热反应生成Cl2的体积约为2.24 L |