题目内容
20.硒(Se)是人体健康必需的一种微量元素.已知Se的原子结构示意图为: 下列说法不正确的是( )
下列说法不正确的是( )| A. | 该原子的质量数为34 | B. | 该元素处于第四周期第ⅥA族 | ||
| C. | SeO2既有氧化性又有还原性 | D. | 酸性:HClO4>H2SeO4 |
分析 A.质量数=质子数+中子数,质子数=原子序数;
B.主族元素原子电子层数=周期数,最外层电子数=族序数;
C.中间价态的元素既有氧化性又有还原性;
D.元素非金属性越强,最高价态氧化物的水化物的酸性越强.
解答 解:A.质量数=质子数+中子数,质子数=原子序数,该原子的质子数为34,所以其质量数大于34,故A错误;
B.主族元素原子电子层数=周期数,最外层电子数=族序数,所以该元素处于第四周期第ⅥA族,故B正确;
C.中间价态的元素既有氧化性又有还原性,二氧化硒中硒处于+4价,是中间价态,所以二氧化硒既有氧化性又有还原性,故C正确;
D.元素非金属性越强,最高价态氧化物的水化物的酸性越强,Cl的非金属性大于Se的非金属性,所以酸性:HClO4>H2SeO4,故D正确.
故选A.
点评 本题考查了元素周期表和元素周期律,明确元素周期律内涵是解本题的关键,知道非金属性的判断方法和原子构成,即可解答.

练习册系列答案
相关题目
10.某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果不正确的是( )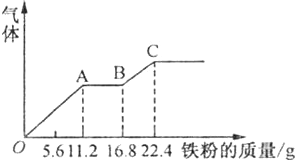

| A. | 图中,AB段的反应为Fe+2Fe 3+=3Fe 2+,溶液中溶质最终为FeSO 4 | |
| B. | 原溶液中H2SO4浓度为2.5mol•L -1 | |
| C. | 原混合溶液中NO3-的物质的量为0.4mol | |
| D. | 图中,OA段产生的气体是NO,BC段产生的气体是氢气 |
11.下列各对原子序数的原子不能以共价键结合成化合物的是( )
| A. | 9和1 | B. | 14和17 | C. | 11和l | D. | 6和17 |
8.下列树脂在一定条件下不能制成塑料的是( )
| A. | 聚乙烯 | B. | 聚氯乙烯 | C. | 酚醛树脂 | D. | 聚四氟乙烯 |
15.下列离子方程式正确的是( )
| A. | 碳酸镁固体与稀硫酸反应:MgCO3+2H++2SO42-═MgSO4+CO2↑+H2O | |
| B. | 碳酸钠溶液与足量氯水反应:CO32-+Cl2═CO2↑+Cl-+ClO- | |
| C. | 碳酸氢铵溶液中加足量氢氧化钡溶液:NH4++HCO3-+2OH-═CO32-+NH3•H2O+H2O | |
| D. | 酸性条件下KClO3和草酸(H2C2O4)生成高效消毒杀菌剂ClO2: 2ClO3-+H2C2O4+2H+═2ClO2↑+2CO2↑+2H2O |
12.浓度为0.1mol•L-1的醋酸溶液用水稀释后,下列说法错误的是( )
| A. | c(OH-)增大 | B. | H+数目增多 | C. | c(H+)增大 | D. | 导电性减弱 |
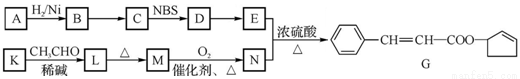
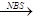 CH3CHBrCH=CH2
CH3CHBrCH=CH2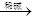
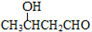 、
、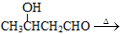 CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O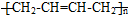 )的合成路线:___________________________。
)的合成路线:___________________________。