题目内容
等物质的量的Na、Mg、Al分别与1L 1mol/L的盐酸反应,产生的气体体积在相同状况下分别为VNa、VMg、VAl,设金属的物质的量为x,当x取不同数值时,填写表格(1)(2)处产生的氢气的体积关系,及表中(3)(4)处x的取值范围.
| Na、Mg、Al等物质的量 x mol | x<
|
| (3) | (4) | ||||
| H2的体积 | (1) | (2) | VNa>VMg=VAl | VNa=VMg=VAl |
考点:化学方程式的有关计算,有关范围讨论题的计算
专题:几种重要的金属及其化合物
分析:三种金属与盐酸反应的方程式分别为:2Na+2HCl=2NaCl+H2↑、Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑,HCl的物质的量为1L×1mol/L=1mol,盐酸完全反应生成生成氢气为1mol×
×22.4L/mol=11.2L,由方程式可知,此时需要Na为1mol、Mg为0.5mol,Al为
mol,而盐酸不足时Na继续与水反应生成氢气,故生成氢气体积与金属物质的量关系图为: ,结合图象分析计算.
,结合图象分析计算.
| 1 |
| 2 |
| 1 |
| 3 |
 ,结合图象分析计算.
,结合图象分析计算.解答:
解:三种金属与盐酸反应的方程式分别为:2Na+2HCl=2NaCl+H2↑、Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑,HCl的物质的量为1L×1mol/L=1mol,盐酸完全反应生成生成氢气为1mol×
×22.4L/mol=11.2L,由方程式可知,此时需要Na为1mol、Mg为0.5mol,Al为
mol,而盐酸不足时Na继续与水反应生成氢气,故生成氢气体积与金属物质的量关系图为: ,则:
,则:
①当x<
时,产生氢气体积:V(Al)>V(Mg)>V(Na);
②当
≤x<1时,产生氢气体积:V(Al)=V(Mg)>V(Na);
③当x=1时,产生氢气体积:V(Al)=V(Mg)=V(Na);
④当x>1时,产生氢气体积:V(Al)=V(Mg)<V(Na);
故答案为:
.
| 1 |
| 2 |
| 1 |
| 3 |
 ,则:
,则:①当x<
| 1 |
| 2 |
②当
| 1 |
| 2 |
③当x=1时,产生氢气体积:V(Al)=V(Mg)=V(Na);
④当x>1时,产生氢气体积:V(Al)=V(Mg)<V(Na);
故答案为:
| Na、Mg、Al等物质的量 x mol | x<
|
| x>1 | x=1 | ||||
| H2的体积 | V(Al)>V(Mg)>V(Na) | V(Al)=V(Mg)>V(Na) | VNa>VMg=VAl | VNa=VMg=VAl |
点评:本题考查范围讨论题的有关计算,明确物质恰好反应的分界点是解本题关键,利用图象找出生成气体体积与金属物质的量的关系,一目了然、化繁为简,题目难点中等.

练习册系列答案
相关题目
能证明SO2具有漂白性的是( )
| A、溴水中通入SO2气体后溶液褪色 |
| B、酸性KMnO4溶液中通入SO2气体后溶液褪色 |
| C、品红溶液中通入SO2气体后溶液褪色 |
| D、滴有酚酞的NaOH溶液中通入SO2气体后溶液褪色 |
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-,现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.792L(已换算成标准状况,且设气体全部逸出);②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.根据上述实验,以下推测正确的是( )
| A、一定不存在Ba2+,NH4+可能存在 |
| B、一定不存在Cl- |
| C、一定存在Na+ |
| D、可能存在Cl-、Na+ |
某废水含有下列离子中的5种(忽略水的电离及离子的水解),K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,测得各种离子的物质的量浓度相等.为探究废水的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
| A、溶液中无法确定Al3+的存在与否 |
| B、原溶液中不含的离子为:K+、Al3+、CO32- |
| C、步骤②中可以确定Fe2+、NO3-的存在 |
| D、步骤③中共有2种钡盐沉淀 |
石灰石是一种化工原料,可以通过反应生成一系列物质,如图.
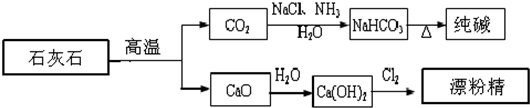
下列说法正确的是( )

下列说法正确的是( )
| A、漂粉精是混合物,主要成分是氯化钙 |
| B、图示的制纯碱方法,要求先向饱和食盐水中通NH3,然后再通CO2 |
| C、纯碱属于碱,俗名苏打 |
| D、制取纯碱和漂粉精所涉及的反应都是非氧化还原反应 |