题目内容
16.设NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 电解精炼铜时,阳极质量减少6.4g,电路中电子转移的总数为0.2NA | |
| B. | 6.0gSiO2晶体中含有0.2NA个Si-O键 | |
| C. | NA个CH4在标准状况下的体积约为22.4L | |
| D. | 苯与液溴反应生成1mol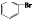 时消耗0.5NA个Br2 时消耗0.5NA个Br2 |
分析 A、电解精炼铜时,阳极上放电的不止是铜;
B、求出二氧化硅的物质的量,然后根据1mol二氧化硅中含4mol硅氧键来分析;
C、气体体积V=$\frac{N}{{N}_{A}}{V}_{m}$来分析;
D、苯和液溴反应时,取代1molH原子消耗1mol溴.
解答 解:A、电解精炼铜时,阳极上放电的不止是铜,还有比铜活泼的金属,故当阳极减少6.4g时,转移的电子数多于0.2NA个,故A错误;
B、6.0g二氧化硅的物质的量为0.1mol,而1mol二氧化硅中含4mol硅氧键,故0.1mol二氧化硅中含0.4NA个硅氧键,故B错误;
C、气体体积V=$\frac{N}{{N}_{A}}{V}_{m}$=$\frac{{N}_{A}}{{N}_{A}/mol}×22.4mol/L$=22.4L,故C正确;
D、苯和液溴反应时,取代1molH原子消耗1mol溴,故当生成1mol溴苯时消耗1mol溴即NA个溴,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
6.下列关于各图象与对应的叙述不相符合的是( )
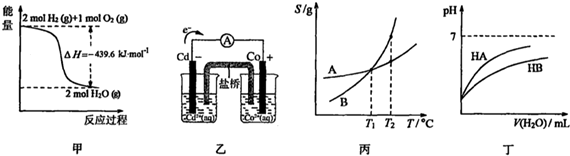

| A. | 由甲可知:氢气的燃烧热为219.8kJ/mol | |
| B. | 由乙可知:盐桥中的Cl-向Cd电极移动 | |
| C. | 由丙可知:将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数:A=B | |
| D. | 由丁可知:同温度、同浓度的NaA溶液与NaB溶液相比,其PH:NaA<NaB |
7.常温下,pH=9的NaOH溶液和Na2S溶液,由水电离出的c(H+)分别为x mol/L、y mol/L,两者关系是( )
| A. | x<y | B. | x>y | C. | x﹦y | D. | 无法判断 |
4.下列说法正确的是( )
| A. | 蛋白质的水解可用于分离和提纯蛋白质 | |
| B. | 丙烯酸甲酯可通过缩聚反应生成高分子化合物 | |
| C. | 有机物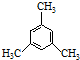 的核磁共振氢谱有两个峰,且峰面积之比为3:1 的核磁共振氢谱有两个峰,且峰面积之比为3:1 | |
| D. | 用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度 |
11.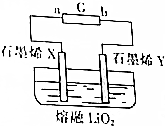 据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )
据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )
 据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )
据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )| A. | 充电过程,电源G的b极为负极 | |
| B. | 放电过程,Y极发生还原反应 | |
| C. | 放电过程,X极的电极反应式为Li-e-+O2-═LiO2 | |
| D. | 充电过程,每转移2 mol电子,Y极放出44.8L(标准状况)O2 |
5.下列烯烃中存在顺反异构体的是( )
| A. | 丙烯 | B. | 1-丁烯 | C. | 1-戊烯 | D. | 3-甲基-2-戊烯 |
19.下列有关摩尔使用的说法中不正确的是( )
| A. | 1mol O | B. | 1mol O2 | C. | 1mol氧原子 | D. | 1摩尔小麦 |
 .
.