题目内容
4.美国通用原子能公司(GA)提出的碘硫热化学循环是由反应Ⅰ、Ⅱ、Ⅲ三步反应组成的(如图所示),下列有关说法正确的是( )
| A. | 设计该循环是为了制取能源气体O2 | |
| B. | 整个循环过程中产生1mol O2的同时产生44.8LH2 | |
| C. | 图中反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 | |
| D. | 图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行 |
分析 由图可知,反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI,该反应为SO2+2H2O+I2=H2SO4+2HI,反应Ⅲ是2HI$\frac{\underline{\;\;△\;\;}}{\;}$H2↑+I2↑,反应Ⅱ是硫酸分解为氧气的过程,据此回答.
解答 解:A、设计该循环是为了制取气体O2和H2,故A错误;
B、整个循环过程中产生1molO2的同时产生标况下44.8LH2,故B错误;
C、反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI,该反应为SO2+2H2O+I2=H2SO4+2HI,反应Ⅲ是2HI$\frac{\underline{\;\;△\;\;}}{\;}$H2↑+I2↑,反应Ⅱ是硫酸分解为氧气的过程,均为氧化还原反应,故C正确;
D、反应Ⅱ、Ⅲ不可在常温常压下进行,反应SO2+2H2O+I2=H2SO4+2HI可以在常温下进行,故D错误.
故选C.
点评 本题涉及物质的转化和氧化还原反应的有关知识,注意知识的归纳和梳理是解题的关键,难度中等.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案
相关题目
3.下列方程式书写正确的是( )
| A. | 除去锅炉的水垢:CaCO3+SO42-?CaSO4+CO32- | |
| B. | 电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 实验室制氯气:KClO3+6H37Cl(浓)═KCl+337Cl2↑+3H2O | |
| D. | HCO3-的水解:HCO3-+H2O?CO32-+H3O+ |
9.在盛有1mL 1mol•L-1AlCl3溶液的试管中加入2mL10%的NH4F溶液,再加入1mL 3mol•L-1氨水,没有生成白色沉淀,其原因是( )
| A. | 溶液的碱性太弱 | B. | Al3+不与氨水反应 | ||
| C. | 生成的Al(OH)3溶解了 | D. | Al3+几乎都与F-结合生成了新物质 |
16.下列各组物质混合后,不能同时产生无色气体和白色沉淀的是( )
| A. | 少量过氧化钠投入AlCl3溶液 | B. | FeCl3溶液与NaHCO3溶液混合加热 | ||
| C. | Ba(OH)2溶液与(NH4)2SO4 | D. | 明矾溶液与小苏打溶液混合 |
13.下列过程涉及化学变化的是( )
| A. | 酒香四溢 | B. | 海带制碘 | C. | 石油分馏 | D. | 萃取分液 |
 ,下列可以验证C与D两元素原子得电子能力强弱的事实是BCD(填编号).
,下列可以验证C与D两元素原子得电子能力强弱的事实是BCD(填编号).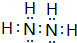 ;C的另一种氢化物与D的一种氢化物的电子总数相等,实验室制取C的该气态氢化物的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
;C的另一种氢化物与D的一种氢化物的电子总数相等,实验室制取C的该气态氢化物的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
 .
. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O
+H2O

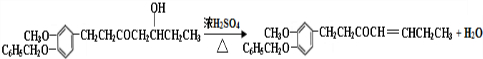 .
. 或
或 ,1mol该物质在一定条件下与足量的NaOH溶液反应,需要的NaOH的物质的量是3或2mol.
,1mol该物质在一定条件下与足量的NaOH溶液反应,需要的NaOH的物质的量是3或2mol.